Фазовые и агрегатные состояния вещества с макроскопической и микроскопической точек зрения, Агрегатные состояния вещества: факты, теории, гипотезы. |

|
Здравствуйте, гость ( Вход | Регистрация )
  |
Фазовые и агрегатные состояния вещества с макроскопической и микроскопической точек зрения, Агрегатные состояния вещества: факты, теории, гипотезы. |
 6.12.2018, 10:12 6.12.2018, 10:12
Сообщение
#101
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
Так вот и дайте расчет, только обоснуйте все исходные данные и понятия со ссылками на источники. В частности, надо обосновать, что принято считать расстоянием между атомами и молекулами, а не заниматься самодеятельностью. Извольте: Расчёт межатомных и межмолекулярных расстояний в твёрдых телах (xls 15 kb) Из этого расчёта получается, что расстояния между центрами атомов алюминия в 1,36 раза меньше чем расстояния между центрами молекул корунда, состоящих не из одного, а из пяти атомов. Соответственно объём, занимаемый одним атомом алюминия всего в 2,5 раза меньше, чем объём занимаемый 5 атомами молекулы корунда. Если сложить теннисные мячи максимально плотно, то объём занимаемый сотней таких мячей будет в пять раз меньше, чем занимаемый пятьюстами. В пять, а не в 2,5! Где деньги, Зин? |

|
|
 6.12.2018, 15:17 6.12.2018, 15:17
Сообщение
#102
|
|
 Младший сержант    Группа: Старожилы Сообщений: 1961 Регистрация: 24.1.2018 Пользователь №: 145544 |
|

|
|
 6.12.2018, 16:10 6.12.2018, 16:10
Сообщение
#103
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
 Кроме как по комиксам, поколение ЕГЭ изучать физику принципиально не может. Размеры атомов кислорода ничуть не меньше, чем размеры атомов алюминия. Док-во плотность кислорода в жидкой и твёрдой фазах. В жидкой 1,41 г/см3, в твёрдой 1,27 г/см3. Т.е. один моль (6,022*1023 атомов кислорода) в твёрдой фазе занимают такой же объём, как и один моль алюминия. А в комиксе атомы кислорода нарисованы в разы меньшими атомов алюминия. |

|
|
 6.12.2018, 20:44 6.12.2018, 20:44
Сообщение
#104
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
Четыре с лишком часа уже прошло, а "германа" всё нет.
В своём ответе я лажанулся, написав, что 6,022*1023 атомов кислорода занимают такой же объём в твёрдой фазе, как и столько же атомов алюминия. Правильно было написать, что 6,022*1023 молекул , а не атомов кислорода занимают такой же объём как один моль алюминия. Хотел было сразу исправить, но потом подумал, а как "поколение ЕГЭ и пепси" среагирует на мою лажу? Получается, что проглотило не поперхнувшись, как до этого глотало комиксы. Вот такие знания у этого хамоватого и охочего до картинок поколения. |

|
|
 6.12.2018, 21:52 6.12.2018, 21:52
Сообщение
#105
|
|
|
Старший сержант      Группа: Старожилы Сообщений: 3082 Регистрация: 2.9.2017 Из: г. Нью-Йорк, США Пользователь №: 78622 |
Цитата Четыре с лишком часа уже прошло, а "германа" всё нет А разница во времени с Москвой у меня 8 часов и можно еще подумать, что у меня с утра больше других дел нет как сидеть на форуме. Теперь по поводу ссылки. Совершенно непонятен источник. да и расчета нет никакого. Каждая цифра должна быть обоснована источником, откуда она взята. Нет и самого расчета а приведены только его результаты. И еще : термин расстояние между атомами или молекулами должен иметь дефиницию. Если это межъядерное расстояние, то так лучше его и называть, а если это расстояние между молекулами или атомами - это зазор или перекрытие (взаимопроникновение) или зазор со знаком минус. |

|
|
 7.12.2018, 2:22 7.12.2018, 2:22
Сообщение
#106
|
|
 Младший сержант    Группа: Старожилы Сообщений: 1961 Регистрация: 24.1.2018 Пользователь №: 145544 |
Тут столько лажи, что и разбираться в этом говне не хочется.
Почитали бы сначала хоть что такое число Авогадро, а потом подумали, а потом написали. Сначала написал лажу, потом попытался исправить и снова лажанулся. Варяг, бросайте эту физику, ну не ваше это... совсем не ваше. |

|
|
 7.12.2018, 7:11 7.12.2018, 7:11
Сообщение
#107
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
А разница во времени с Москвой у меня 8 часов и можно еще подумать, что у меня с утра больше других дел нет как сидеть на форуме.http://xn----8sbbemc3a7aecex.xn--p1ai/forum/style_images/ip.boardpr/folder_editor_images/rte-switch-editor.png Теперь по поводу ссылки. Совершенно непонятен источник. да и расчета нет никакого. Каждая цифра должна быть обоснована источником, откуда она взята. Нет и самого расчета а приведены только его результаты. И еще : термин расстояние между атомами или молекулами должен иметь дефиницию. Если это межъядерное расстояние, то так лучше его и называть, а если это расстояние между молекулами или атомами - это зазор или перекрытие (взаимопроникновение) или зазор со знаком минус. Похоже, Вы не в курсе, как делаются вычисления в Excel, и где находятся расчётные формулы. А что касается исходных данных, то они взяты из открытых источников, которые доступны всем, например, из не любимой мной википедии. Касаемо расстояний межу атомами, то конечно, можно взять и межъядерное, но что тогда считать межъядерным для молекул? Поэтому, правильнее, на мой взгляд, брать не расстояние, а объём занимаемый атомом или молекулой. Разделив объём моля вещества на число Авогадро, получим объём занимаемый атомом или молекулой с учётом зазоров между ними. P.S. Моё "А "германа" всё нет" адресовалась, отнюдь, не Вам, а представителю поколения ЕГЭ и пепси, к которому Вас нельзя причислить, поскольку в школу Вы пошли сразу после войны. |

|
|
 7.12.2018, 13:50 7.12.2018, 13:50
Сообщение
#108
|
|
 Младший сержант    Группа: Старожилы Сообщений: 1961 Регистрация: 24.1.2018 Пользователь №: 145544 |
Неужели я услышал слово моль. Но слово объём снова меня смущает. Разве у молей известны объёмы... А не считается ли число Авогадро через известный объём вещества?
Digger, Не стройте из себя психолога, тут вы тоже ноль! Цитата В 1938 году Pepsi Cola Company (впоследствии — PepsiCo) зарегистрировала право исключительного пользования товарным знаком на территории Советского Союза в Бюро по регистрации товарных знаков Наркомторга СССР. Впервые советские граждане смогли массово попробовать напиток в 1959 году на выставке «Промышленная продукция США» в московском парке Сокольники. В ходе выставки вице-президент США Ричард Никсон по просьбе президента компании PepsiCo International Дональда Кендалла угостил «пепси» советского лидера Никиту Хрущева. Разве вы на столько старый, что не попадаете под поколение пепси? Сообщение отредактировал ahedron - 7.12.2018, 13:54 |

|
|
 7.12.2018, 17:46 7.12.2018, 17:46
Сообщение
#109
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
Неужели я услышал слово моль. Но слово объём снова меня смущает. Разве у молей известны объёмы... А не считается ли число Авогадро через известный объём вещества? Digger, Не стройте из себя психолога, тут вы тоже ноль! Разве вы на столько старый, что не попадаете под поколение пепси? Поскольку поколение ЕГЭ в вашем лице, не знает что такое моль, то дабы другие не были введены в заблуждение вашими безграмотными экзерсисами, считаю своим долгом объяснить вам и вам подобным, что моль, по определению - количество вещества в граммах, численно равном его атомному или молекулярному весу. Объём одного моля рассчитывается исходя из его веса и плотности вещества. Т.е. объём 1 моля любого вещества есть вес этого моля делённый на плотность этого вещества. Число Авогадро легко рассчитать зная атомную (молекулярную) массу вещества и массу нуклонов составляющих атом или молекулу этого вещества. Не существует никакого иного способа точно вычислить число Авогадро. Т.е. ваше утверждение "А не считается ли число Авогадро через известный объём вещества?" - свидельство вашей вопиющей безграмотности и неимоверного самомнения и наглости. Видимо, одно является следствием другого. Через объём вещества (газа) число Авогадро пытались вычислить ещё в середине 19-го века, но точность этих вычислений была крайне невысокой. И только в 20-м веке, когда научились измерять массу ядер и нуклонов, учёные смогли вычислить современное значение числа Авогадро. |

|
|
 7.12.2018, 19:29 7.12.2018, 19:29
Сообщение
#110
|
|
 Младший сержант    Группа: Старожилы Сообщений: 1961 Регистрация: 24.1.2018 Пользователь №: 145544 |
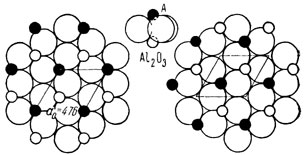
Вы хотите сказать этой темой, что молекула корунда это куб? как и все молекулы вообще, даже ДНК у вас куб... хм... интересное заявление.
|

|
|
 7.12.2018, 20:09 7.12.2018, 20:09
Сообщение
#111
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
|

|
|
 7.12.2018, 21:00 7.12.2018, 21:00
Сообщение
#112
|
|
 Младший сержант    Группа: Старожилы Сообщений: 1961 Регистрация: 24.1.2018 Пользователь №: 145544 |
Цитата Если сложить теннисные мячи максимально плотно, то объём занимаемый сотней таких мячей будет в пять раз меньше, чем занимаемый пятьюстами.
|

|
|
 7.12.2018, 21:21 7.12.2018, 21:21
Сообщение
#113
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
А вы, видимо считаете, что 500 мячей займут объём не в 5 раз бОльший, нежели сто точно таких же мячей?
Ну и во сколько же раз, по вашему? |

|
|
 8.12.2018, 7:27 8.12.2018, 7:27
Сообщение
#114
|
|
|
Старший сержант      Группа: Старожилы Сообщений: 3082 Регистрация: 2.9.2017 Из: г. Нью-Йорк, США Пользователь №: 78622 |
Если речь идет о молекулах, то размеры их зависят не только от химического состава, но и от строения и характера связей между атомами. Молекулы могут состоять из атомов одного элемента, например, газы Н₂, О₂, в которых электронные облака сближаются и взаимно пересекаются. Эта связь называется ковалентной. Читайте последний абзац на стр. 114 и см. рис. 26, 27 приложения. (Глинка, Общая химия)
[attachment=268:p0137.png] Связь может быть ионной, когда молекула состоит из атомов различных элементов, причем один из атомов - щелочной металл, например, Na легко отдает свой электрон из наружного слоя, превращаясь в положительно заряженный ион Na+, а другой элемент - сильный электроотрицательный металлоид - Cl, принимает его в свои объятья и образует отрицательно заряженный ион Cl- . Оба иона, имеющие противоположные заряды, притягиваются друг к другу, образуя молекулу NaCl. Соединившись в молекулу, два разноименно заряженных иона сохраняют свою способность взаимодействовать с другими молекулами, так как представляют собой систему из двух одинаковых по величине, но противоположных по знаку зарядов, создающих электрическое поле. Вот вам и "нейтральные молекулы" ( в среднем по колхозу). Возвращаясь к ковалентной связи (рис. 27) следует отметить , что химическая связь двух атомов водорода является результатом взаимопроникновения (перекрывания) электронных облаков, происходящего при сближении атомов. Вследствие такого перекрывания плотность отрицательного заряда в межъядерном пространстве возрастает, а положительно заряженные ядра притягиваются к области перекрывания электронных облаков. Это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов и таким образом образуется молекула. Как видите, приведенные два способа образования молекул принципиально различны. Но это не все. Есть и другие типы связей. Расмотрим их в следующий раз. А пока что отметим, что атом практически пуст и его электронное облако может деформироваться при образовании молекул. |

|
|
 8.12.2018, 8:53 8.12.2018, 8:53
Сообщение
#115
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
Если речь идет о молекулах, то размеры их зависят не только от химического состава, но и от строения и характера связей между атомами. Молекулы могут состоять из атомов одного элемента, например, газы Н₂, О₂, в которых электронные облака сближаются и взаимно пересекаются. Эта связь называется ковалентной. Читайте последний абзац на стр. 114 и см. рис. 26, 27 приложения. (Глинка, Общая химия) [attachment=268:p0137.png] Связь может быть ионной, когда молекула состоит из атомов различных элементов, причем один из атомов - щелочной металл, например, Na легко отдает свой электрон из наружного слоя, превращаясь в положительно заряженный ион Na+, а другой элемент - сильный электроотрицательный металлоид - Cl, принимает его в свои объятья и образует отрицательно заряженный ион Cl- . Оба иона, имеющие противоположные заряды, притягиваются друг к другу, образуя молекулу NaCl. Соединившись в молекулу, два разноименно заряженных иона сохраняют свою способность взаимодействовать с другими молекулами, так как представляют собой систему из двух одинаковых по величине, но противоположных по знаку зарядов, создающих электрическое поле. Вот вам и "нейтральные молекулы" ( в среднем по колхозу). Возвращаясь к ковалентной связи (рис. 27) следует отметить , что химическая связь двух атомов водорода является результатом взаимопроникновения (перекрывания) электронных облаков, происходящего при сближении атомов. Вследствие такого перекрывания плотность отрицательного заряда в межъядерном пространстве возрастает, а положительно заряженные ядра притягиваются к области перекрывания электронных облаков. Это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов и таким образом образуется молекула. Как видите, приведенные два способа образования молекул принципиально различны. Но это не все. Есть и другие типы связей. Расмотрим их в следующий раз. А пока что отметим, что атом практически пуст и его электронное облако может деформироваться при образовании молекул. Двигаться нужно от простого к сложному, а Вы нагородили здесь ионные, коваоентные связи, заряды. Вы сами-то никогда не задумывались над абсурдностью современных представлений о химической связи, образованной т.н. "валентными электронами". Считается, что электроны - отрицательно заряжены, а из этого следует, что они не млгут спариваться, но только отталкиваться. Не химия, а какой-то гей-парад а Вашингтоне. Давайте попробуем абстрагироваться от химических связей, и посмотреть на строение в-ва с другой стороны: Вам наверняка известно, что углерод может существовать в трёх различных аллотропных модификациях: сажа, графит и алмаз. За каким лешим электронам двух атомов углерода нужно спариваться, если атомы углерода и так электронейтральны? Давайте попробуем посмотреть на строение молекул с другой стороны: Поскольку Вы знаете и понимаете термодинамику, то Вас наверняка должен заинтересовать вопрос о том, почему теплоёмкость выше перечисленных аллотропных модификаций существенно различается. Так, например, мольная теплоёмкость алмаза составляет примерно 6 Дж/моль*К, графита 8, а сажи 25 Дж/моль*К ! Любопытная получается картина: в алмазе самые прочные связи, т.е. на раскачку атома углерода в алмазе нужно затратить больше энергии, нежели в графите, и уж тем болеее в саже. Но видим-то мы совсем иное! Как,по-Вашему, можно объяснить сей неоспоримый факт? Или другой пример: Теплоёмкость воды в твёрдом (лёд) и газообразном (пар) агрегатном состоянии одинакова, а вот в жидкой фазе её теплоёмкость выше в 2,5 раза. Вопрос: какая-такая дополнительная степень свободы, которой не было у неё в парообразном состоянии, появилась в состоянии жидком?! Для ртути теплоёмкость примерно одинакова, как для твёрдой, так для жидкой и парообразной фаз. Для всех, подчёркиваю, для всех простых (одноатомных) в-в теплоёмкомкость примерно одинакова для всех агрегатных состояний, разумеется, только, если температура этих агрегатных состояний различается не на несколько сотен и больше градусов. При низких температурах теплоёмкость плавно уменьшается, а при увеличении температуры плавно увеличивается. А вот у сложных веществ, молекула которых состоит из нескольких атомов, теплоёмкость в жидкой фазе скачком увеличивается в разы, по сравнеию с другими фазами. Сей факт современная наука стыдливо обходит молчанием. На мой взгляд, объяснение этого феномена следует искать в строении вещества (строении молекулы). Ну а поскольку современные представления о строении молекулы не дают возможности внятно и непротиворечиво объяснить феномен скачкообразного увеличения теплоёмкости сложных в-в в жидкой фазе, то есть все основания для сомнений в правильности существующих представлений о строении молекулы, да и молекулярно-кинетической теории тоже. |

|
|
 8.12.2018, 17:17 8.12.2018, 17:17
Сообщение
#116
|
|
 Младший сержант    Группа: Старожилы Сообщений: 1549 Регистрация: 13.11.2017 Из: Из Воркуты Пользователь №: 200194 |
ВСе теории неверны, иначе и быть не может.
-------------------- Вышли из печати книжка "Гравитация" https://www.litres.ru/evgeniy-alekseevich-/gravitaciya-novaya-paradigma-seriya-fizika-vysokorazv/
|

|
|
 9.12.2018, 4:26 9.12.2018, 4:26
Сообщение
#117
|
|
|
Старший сержант      Группа: Старожилы Сообщений: 3082 Регистрация: 2.9.2017 Из: г. Нью-Йорк, США Пользователь №: 78622 |
Цитата Двигаться нужно от простого к сложному, а Вы нагородили здесь ионные, коваоентные связи, заряды. Вы тут нагородили сорок бочек арестантов и на все вопросы я должен отвечать? Ответьте мне на один простой вопрос, чтобы мы могли двигаться дальше Вы всерьёз отрицаете существование ионов? Да или нет?
|

|
|
 9.12.2018, 6:32 9.12.2018, 6:32
Сообщение
#118
|
|
|
Младший сержант    Группа: Старожилы Сообщений: 1189 Регистрация: 17.11.2018 Пользователь №: 200577 |
Вы тут нагородили сорок бочек арестантов и на все вопросы я должен отвечать? Ответьте мне на один простой вопрос, чтобы мы могли двигаться дальше Вы всерьёз отрицаете существование ионов? Да или нет? Существование ионов, как ионизированных атомов и молекул, конечно, же не отрицаю. Ответьте на один мой простой вопрос, чтобы мы могли даигаться дальше: Как объяснить скачкообразное увеличение теплоёмкости сложных в-в в жидкой фазе? |

|
|
 9.12.2018, 8:57 9.12.2018, 8:57
Сообщение
#119
|
|
|
Ефрейтор   Группа: Старожилы Сообщений: 782 Регистрация: 9.10.2017 Пользователь №: 99655 |
Двигаться нужно от простого к сложному, а Вы нагородили здесь ионные, коваоентные связи, заряды. Вы сами-то никогда не задумывались над абсурдностью современных представлений о химической связи, образованной т.н. "валентными электронами". Считается, что электроны - отрицательно заряжены, а из этого следует, что они не млгут спариваться, но только отталкиваться. Не химия, а какой-то гей-парад а Вашингтоне. Давайте попробуем абстрагироваться от химических связей, и посмотреть на строение в-ва с другой стороны: Вам наверняка известно, что углерод может существовать в трёх различных аллотропных модификациях: сажа, графит и алмаз. За каким лешим электронам двух атомов углерода нужно спариваться, если атомы углерода и так электронейтральны? Давайте попробуем посмотреть на строение молекул с другой стороны: Поскольку Вы знаете и понимаете термодинамику, то Вас наверняка должен заинтересовать вопрос о том, почему теплоёмкость выше перечисленных аллотропных модификаций существенно различается. Так, например, мольная теплоёмкость алмаза составляет примерно 6 Дж/моль*К, графита 8, а сажи 25 Дж/моль*К ! Любопытная получается картина: в алмазе самые прочные связи, т.е. на раскачку атома углерода в алмазе нужно затратить больше энергии, нежели в графите, и уж тем болеее в саже. Но видим-то мы совсем иное! Как,по-Вашему, можно объяснить сей неоспоримый факт? Или другой пример: Теплоёмкость воды в твёрдом (лёд) и газообразном (пар) агрегатном состоянии одинакова, а вот в жидкой фазе её теплоёмкость выше в 2,5 раза. Вопрос: какая-такая дополнительная степень свободы, которой не было у неё в парообразном состоянии, появилась в состоянии жидком?! Для ртути теплоёмкость примерно одинакова, как для твёрдой, так для жидкой и парообразной фаз. Для всех, подчёркиваю, для всех простых (одноатомных) в-в теплоёмкомкость примерно одинакова для всех агрегатных состояний, разумеется, только, если температура этих агрегатных состояний различается не на несколько сотен и больше градусов. При низких температурах теплоёмкость плавно уменьшается, а при увеличении температуры плавно увеличивается. А вот у сложных веществ, молекула которых состоит из нескольких атомов, теплоёмкость в жидкой фазе скачком увеличивается в разы, по сравнеию с другими фазами. Сей факт современная наука стыдливо обходит молчанием. На мой взгляд, объяснение этого феномена следует искать в строении вещества (строении молекулы). Ну а поскольку современные представления о строении молекулы не дают возможности внятно и непротиворечиво объяснить феномен скачкообразного увеличения теплоёмкости сложных в-в в жидкой фазе, то есть все основания для сомнений в правильности существующих представлений о строении молекулы, да и молекулярно-кинетической теории тоже. Убедительно... |

|
|
 11.12.2018, 7:25 11.12.2018, 7:25
Сообщение
#120
|
|
|
Старший сержант      Группа: Старожилы Сообщений: 3082 Регистрация: 2.9.2017 Из: г. Нью-Йорк, США Пользователь №: 78622 |
Цитата Двигаться нужно от простого к сложному, а Вы нагородили здесь ионные, коваоентные связи, заряды. Вы сами-то никогда не задумывались над абсурдностью современных представлений о химической связи, образованной т.н. "валентными электронами". Считается, что электроны - отрицательно заряжены, а из этого следует, что они не млгут спариваться, но только отталкиваться. Не химия, а какой-то гей-парад а Вашингтоне. thumbsdown.gif Цитата Существование ионов, как ионизированных атомов и молекул, конечно, же не отрицаю. Ответьте на один мой простой вопрос, чтобы мы могли даигаться дальше: Как объяснить скачкообразное увеличение теплоёмкости сложных в-в в жидкой фазе? Вот я привел две цитаты Diggerа. Неужели вы не видите в них непоследовательности и противоречия? Если вы не отрицаете существования ионов и считаете абсурдностью химическую связь "валентными электронами" и утверждаете, что электроны как одинаково заряженные не могут спариваться, а только отталкиваться. Тогда разберем, что такое ион и валентные электроны. Вот определение валентного электрона: В химии валентными электронами называют электроны, находящиеся на внешней (валентной) оболочке атома. А вот определение иона: Ио́н (др.-греч. ἰόν «идущее») — частица, в которой общее число протонов не равно общему числу электронов. Ион, в котором общее число протонов больше общего числа электронов, имеет положительный заряд и называется катионом. Ион, в котором общее число протонов меньше общего числа электронов, имеет отрицательный заряд и называется анионом. Как появляются ионы? Верхняя оболочка атома содержит так называемые валентные электроны, наименее связанные с ядром. В верхней оболочке число электронов не может превышать восьми. Восемь - наиболее устойчивая структура , присущая инертным газам. Если электронов во внешнем слое меньше 4х - атом под влиянием внешних сил может терять свои валентные электроны, превращаясь в положительно заряженный ион, а если более 4х- то принимать (захватывать) чужие электроны, превращаясь в отрицательно заряженный ион. При этом в каждом ионе создается устойчивый наружный слой, состоящий из 8 электронов. Разноименные ионы, например, Na+ и Cl- притягиваются образуя молекулу NaCl - поваренную соль с ионной связью Что же сложного я здесь написал? Это и есть САМОЕ ПРОСТОЕ образование молекул. Хотя атом хлористого натрия в целом представляет нейтральную молекулу, но система двух ионов является системой из двух зарядов , способной создавать электрическое поле. Два иона, притянувшихся друг к другу, обладают способностью электростатически взаимодействовать друг с другом и образовывать кристаллическую решетку. А вы полагаете , что молекулы это нейтральные шарики, сбившиеся в кучу. Это самое примитивное представление о строении твердого тела. На самом деле твердые тела устроены гораздо сложнее. Ионная связь - простейшая из возможных. О ковалентной связи атомов в молекулах одного элемента я уже писал. Существует еще полярная ковалентная связь. Для пояснения ее необходимо приготовить рисунки, а пока я отвечу насчет теплоемкости. Вопрос объяснения теплоемкости различных веществ и фаз не является предметом термодинамики, так как целиком зависит от теорий строения вещества. Существует классическая теория теплоемкости твердых тел, основанная на молекулярной теории, которая правильно описывает определенный круг явлений, но многие явления она не объясняет по причине слишком упощенной модели, принятой в этой теории. Более точные результаты,согласующиеся с опытом дает квантовая теория. Подробнее читайте у Сивухина Курс Физики т.2 стр. 220-227. Вот теперь и смотрите: кто идет от простого к сложному, а кто задает самый сложный вопрос о теплоемкости, на который у науки пока нет однозначного ответа для всех состояний вещества. |

|
|
  |
| Текстовая версия | Сейчас: 26.4.2024, 10:23 |