Версия для печати темы
Нажмите сюда для просмотра этой темы в обычном формате
Форумы Боевого Народа _ ОКолоНАуки _ Фазовые и агрегатные состояния вещества с макроскопической и микроскопической точек зрения
Автор: mechanic 19.11.2018, 8:07
Эта тема открыта в противовес аналогичной, открытой Зиновием в основном разделе НиТа, поскольку считаю, что с самого начала обсуждение стало невозможным из-за позиции топик - стартера, который изначально загнал диспут в русло своих личных воззрений на выдвигаемую проблему и препятствовал (как модератор) высказываниям оппонентов, считая их доводы отклонением от темы. Даже определения агрегатных состояний вещества были признаны не относящимися к обсуждаемому вопросу. Здесь он даже противоречит своему же девизу:
"Тот кто не знает и/или не понимает определений физических понятий - не знает физики."
Возмем хотя бы одну строчку из первого поста топик-стартера:
Это: твёрдое, жидкое и газообразное.
Это утверждение - слишком упрощенное и условное, на уровне младших классов средней школы.
Также упрощенным является утверждение:
Таким образом достигаются температуры затвердевания, разжижения и испарения свойственные для данного вида вещества.
Как ни странно, топик- стартер не учитывает такой фактор как давление, влияющее на агрегатное состояние вещества в неменьшей степени, чем температура, тем самым игнорируя термодинамический подход к данной проблеме.
В этой теме предлагается свободная дискуссия, основанная на научных сведениях по этому вопросу и на идеях участников, относящихся к этой тематике. И начнем ее с определения понятий.
Автор: Digger 19.11.2018, 9:55
"Тот кто не знает и/или не понимает определений физических понятий - не знает физики."
Возмем хотя бы одну строчку из первого поста топик-стартера:
Это утверждение - слишком упрощенное и условное, на уровне младших классов средней школы.
Также упрощенным является утверждение:
Автор видимо не знаком со строением различных видов молекул и типом химических связей между ними. Это вопрос Зиновий также считает не относящимся к теме, а изначально пытается направить дискуссию в сторону своей весьма спорной позиции:
Как ни странно, топик- стартер не учитывает такой фактор как давление, влияющее на агрегатное состояние вещества в неменьшей степени, чем температура, тем самым игнорируя термодинамический подход к данной проблеме.
В этой теме предлагается свободная дискуссия, основанная на научных сведениях по этому вопросу и на идеях участников, относящихся к этой тематике. И начнем ее с определения понятий.
Дуумаю, всеи было бы интересно услышать именно от Вас определения понятий "газ", "жидкость", и "твёрдое тело", поскольку прозвучавшее от Вас в упоминаемой Вами теме, что стекло или хрусталь - это жидкость, мягко говоря, вызывает недоумение.
Автор: ahedron 19.11.2018, 15:52
Стекло аморфное тело и оно имеет вязкость, свойство, которое присуще жидкостям, а вот с хрусталём, по ходу кто-то поторопился, сказав что он жидкость, если брать горный хрусталь, то он кристалл, который не обладает вязкостью, в отличии от промышленного... Как-то так.
Зачем вообще делить вещества на агрегатные состояния, думаю, это чисто общий взгляд на вещи. Если разбираться очень скрупулёзно, то чёткой грани между этими состояниями веществ вряд ли можно обнаружить. Имею виду грань, по которой можно точно сказать, что вот это жидкость, а вот это твёрдое тело. Думаю не об этом нужно спорить.
Автор: vps137 19.11.2018, 17:06
Зачем вообще делить вещества на агрегатные состояния, думаю, это чисто общий взгляд на вещи. Если разбираться очень скрупулёзно, то чёткой грани между этими состояниями веществ вряд ли можно обнаружить. Имею виду грань, по которой можно точно сказать, что вот это жидкость, а вот это твёрдое тело. Думаю не об этом нужно спорить.
Доказательством правоты Ваших слов про стекло может служить эксперимент, который я делал ещё школьником. Стекло режется ножницами как картон. Правда, не на воздухе, а под водой.
Автор: alal 19.11.2018, 17:56
Откуда это предположение - "сами молекулы электрически нейтральны" ? Как могут быть нейтральными протон и расположенный рядом электрон (если они существуют) ?
Да-да, какие-такие внешние электрические поля действуют в приведенном ниже видео на предметы ?
https://www.youtube.com/watch?v=sLGHQHLKgj8
Автор: Digger 19.11.2018, 18:09
Вода, как и любая иная жидкость, принимает форму сосуда, в котором находится, строго следует закону сообщающихся сосудов, а в невесомости принимает форму шара.
А стекло и хрусталь???
Принципиальная разница между жидкостью и твёрдым телом, на мой взгляд, заключается в том, что молекулы жидкости могут без усилия перемещаться друг относительно друга, а молекулы твёрдого тела НЕ МОГУТ!
Автор: mechanic 20.11.2018, 2:49
Сразу скажу, что подход к определению агрегатного состояния - твердое тело неоднозначен. Самое простое определение : твердым телом называется агрегатное состояние вещества, при котором тело сохраняет свой объем и форму. Эти условия, как говорят в математике и логике, являются необходимыми, но недостаточными. Уже в школьных учебниках твердые тела подразделяются на два и даже на три вида: кристаллические, аморфные и композиты.
Примерами кристаллических тел являются чистые металлы, алмаз, кварц, соль, сахарный песок. Характерными макроскопическими особенностями кристаллических тел являются анизотропия - физические свойства кристаллов (механические, электрические) зависят от направления, в котором эти свойства определяются, и температура плавления (при постоянном давлении в определенных пределах).
Аморфные тела изотропны, не имеют четко выраженной температуры плавления и проявляют свойство текучести, то есть ведут себя как очень вязкие жидкости. Примерами аморфных тел являются стекло, смолы, асфальт, леденцы, резина, оргстекло, пластмассы, парафин.
Композиты, упомянутые только в учебнике Касьянова, состоят из различных, связанных между собой материалов, например дерево , бетон, фибергласс. Я бы добавил сюда такие пластмассы как текстолит, гетинакс и т.п.
Однако разновидности твердых тел вышеуказанными определениями не исчерпывается. Существует огромное количество полимерных материалов, не вписывающихся в указанную схему, некоторые из них не могут существовать в жидком и газообразном состоянии, также как дерево, хотя и не являются композитами; существуют также сплавы металлов, например, сталь, которая в определенном температурном диапазоне может представлять собой твердый раствор углерода в железе, а в другом диапазоне - различные кристаллические структуры.Этим вопросам посвящена специальная наука - металловедение.
Далее, есть еще и термодинамический взгляд на агрегатные состояния вещества. С точки зрения термодинамики истинно твердыми веществами являются кристаллические вещества. Аморфные вещества отнесены к вязким жидкостям. Под этим утверждением есть внушительная фактическая база. При нормальных условиях аморфное тело может быть расколото сильным ударом как кристалл, но при постоянном силовом воздействии аморфные тела медленно текут. В старинных зданиях нижняя часть оконного стекла имеет большую толщину, чем верхняя. Кусок битума (асфальта), положенный в воронку, постепенно перетекает в колбу. В аморфных телах медленно тонут тяжелые предметы.
Но главным критерием, по которому различаются истинно твердые (кристаллические) тела отличаются от аморфных - это наличие строго определенной температуры плавления при постоянном давлении. Твердая фаза в кристаллических телах обладает меньшей энергией, чем жидкость на величину, которая называется скрытой теплоты плавления. Это означает, что для перевода твердого тела в жидкое состояние недостаточно нагреть его до температуры плавления. Необходимо подвести еще энергию, чтобы расплавить твердое тело. При этом температура двухфазовой системы будет оставаться постоянной, пока последняя твердая частица не будет расплавлена.
У аморфных тел ничего подобного не происходит. При нагревании они размягчаются и их температура меняется плавно. Никакого энергетического барьера в виде теплоты плавления у аморфных тел нет.
Как-то, но не так. Вы путаете хрустальный бокал с кристаллами горного хрусталя. Горный хрусталь - это кристаллы кварца. Хрустальная посуда - это сорт стекла, содержащего большое количество солей свинца, благодаря которым увеличивается коэффициент преломления стекла, приближающего его к алмазу. Это стекло широко используется в оптических изделиях.
Это была макроскопическая характеристика твердых тел.
О жидкостях и газах поговорим в следующих постах. Там же обсудим агрегатные состояния с молекулярной точки зрения.
Автор: Digger 20.11.2018, 7:03
Примерами кристаллических тел являются чистые металлы, алмаз, кварц, соль, сахарный песок. Характерными макроскопическими особенностями кристаллических тел являются анизотропия - физические свойства кристаллов (механические, электрические) зависят от направления, в котором эти свойства определяются, и температура плавления (при постоянном давлении в определенных пределах).
Аморфные тела изотропны, не имеют четко выраженной температуры плавления и проявляют свойство текучести, то есть ведут себя как очень вязкие жидкости. Примерами аморфных тел являются стекло, смолы, асфальт, леденцы, резина, оргстекло, пластмассы, парафин.
Композиты, упомянутые только в учебнике Касьянова, состоят из различных, связанных между собой материалов, например дерево , бетон, фибергласс. Я бы добавил сюда такие пластмассы как текстолит, гетинакс и т.п.
Однако разновидности твердых тел вышеуказанными определениями не исчерпывается. Существует огромное количество полимерных материалов, не вписывающихся в указанную схему, некоторые из них не могут существовать в жидком и газообразном состоянии, также как дерево, хотя и не являются композитами; существуют также сплавы металлов, например, сталь, которая в определенном температурном диапазоне может представлять собой твердый раствор углерода в железе, а в другом диапазоне - различные кристаллические структуры.Этим вопросам посвящена специальная наука - металловедение.
Далее, есть еще и термодинамический взгляд на агрегатные состояния вещества. С точки зрения термодинамики истинно твердыми веществами являются кристаллические вещества. Аморфные вещества отнесены к вязким жидкостям. Под этим утверждением есть внушительная фактическая база. При нормальных условиях аморфное тело может быть расколото сильным ударом как кристалл, но при постоянном силовом воздействии аморфные тела медленно текут. В старинных зданиях нижняя часть оконного стекла имеет большую толщину, чем верхняя. Кусок битума (асфальта), положенный в воронку, постепенно перетекает в колбу. В аморфных телах медленно тонут тяжелые предметы.
Но главным критерием, по которому различаются истинно твердые (кристаллические) тела отличаются от аморфных - это наличие строго определенной температуры плавления при постоянном давлении. Твердая фаза в кристаллических телах обладает меньшей энергией, чем жидкость на величину, которая называется скрытой теплоты плавления. Это означает, что для перевода твердого тела в жидкое состояние недостаточно нагреть его до температуры плавления. Необходимо подвести еще энергию, чтобы расплавить твердое тело. При этом температура двухфазовой системы будет оставаться постоянной, пока последняя твердая частица не будет расплавлена.
У аморфных тел ничего подобного не происходит. При нагревании они размягчаются и их температура меняется плавно. Никакого энергетического барьера в виде теплоты плавления у аморфных тел нет.
Там где речь идёт о термодинамике, Вы не заморачиваетесь рассмотреннием процессов на микроуровне, ограничиваясь лишь макроскопическим подходом.
А здесь Вас вдруг потянуло в строение вещества.
Давайте ограничимся наболее общими свойствами веществ с точки зрения механики, чтобы провести чёткую грань между газом, жидкостью и твёрдым телом.
В противном случае мы будем до бесконечности искать и находить различные вариации в строении веществ на микроуровне. Например, типы связей между атомами и молекулами твёрдого тела можно разделить на ковалентные, ионные, и ещё кучу других.
Поэтому давайте ограничимся чисто механическим подходом с позиции принципа причинности.
А причиной всех без исключения физических процессов, как известно, является сила.
Мало того, нам известно, что силами действующими между атомами и молекулами, являются т.н. "силы Ван дер Ваальса", которые, во-первых, препятствуют сжатию твёрдых тел и жидкостей (несжимемость), а, во-вторых, не дают телам самопроизвольно разрушиться.
На мой взгляд, силами препятствующими сжатию (сближению атомов и молекул), являются силы отталкивания, а силами, удерживающими атомы и молекулы, являются силы притяжения.
Что, впрочем, известно из курса молекулярной физики:
“Силы притяжения изменяются с расстоянием между центрами молекул как r-n, где n ~ 7. Силы отталкивания убывают с увеличением расстояния между центрами молекул по закону r-m, где m≥ 9, т.е. значительно быстрее, чем силы притяжения. Силы отталкивания преобладают на расстояниях, меньших 10-9 ... 10-10 м, а притяжения - на расстояниях, больших 10-10 ... 10-9 м”.
(Гершензон Е.М. и др. ”Молекулярная физика: Учеб. пособие для студ. высш. пед. учеб. заведений” М.: Издательский центр «Академия», 2000 г.)
Стр. 13.
Какой вывод из этого можно сделать?
1. если силы притяжения и отталкивания уравновешены в некотором интервале расстояний, то это позволяет молекулам без усилия перемещаться (поворачиваться) друг относительно друга, что мы наблюдаем в жидкости.
2. если силы притяжения возрастают с увеличением расстояния быстрее, чем силы отталкивания, то это позволяет молекулам сохранять взаимное положнение (твёрдое тело)
3. если силы отталкивания превалируют над силами притяжения, то это позволяет молекулам удаляться друг от друга без прриложения внешней силы (газ).
Другими словами, агрегатное состояние вещества определяется соотношением сил отталкивания и притяжения.
А отсюда становится понятен и механизм агрегатных превращений вещества при изменении температуры или давления.
Увеличение температуры приводит к увеличению сил отталкивания, к уравновешиванию сил притяжения и отталкивания, и переходу твёрдого тела в жидкое состояние.
Увеличение давления приводит к сближению молекул газа до расстояний на которых силы притяжения и отталкивания становятся сопоставимы по величине, что вызывает превращение газа в жидкость.
Автор: Patent 20.11.2018, 13:08
А моём видении твёрдое тело переходит в жидкость тогда, когда силы притяжения его атомов и молекул друг к другу не способны удерживать себя в том же соседстве под действием сил гравитации.
И здесь следует делать оговорку - при данной температуре.
И оговаривать эту температуру.
Потому как и железо можно сделать жидкостью. Смолу признали жидкостью потому, что она за год выпустила одну каплю. При какой температуре всё это происходило осталось тайной. если бы этот опыт ставился не в центральной Европе, а в Африке, то и капель было больше, а если его ставить на крайнем севере, то и за сотню лет можно капли не дождаться.
В данное время мы обычно всё происходящее относим к обычной температуре, которая нас окружает.
Если тело не теряет свою форму, то его следует относить к твёрдым телам. Но, тогда твёрдые тела следует далее делить по прочностным качествам.
Мягкое, твёрдое, очень твёрдое и т.д.
И если тело начинает течь под действием дополнительной к гравитации силе, то это не должно данное твёрдое тело относить к жидкости.
Вот такое моё мнение.
Автор: Digger 20.11.2018, 13:39
И здесь следует делать оговорку - при данной температуре.
Вот уж в газах, точно нет сил притяжения между молекулами.
Но почему не все газы "при данной температуре" не жидкости?
Что принципиально отличает газ от жидкости, если, по Вашему, и там и там силы притяжения неспособны удерживать молекулы "в том же соседстве"?
Вы когда-нибудь слышали, что усилие воды на разрыв, примерно такое же как усилие на разрыв у сосновой древесины?
Это факт экспериментальный, прямо опровергающий Ваши домыслы о неспособности молекул жидкости удерживать своих соседей.
Видимо, в том-то и дело, что Ваша физика - это результат видЕний, а не анализа экспериментальных фактов.
А видЕния, как известно, возникают в мозгу либо в болезненном состоянии, либо под воздействием галюциногенов.
Автор: Patent 20.11.2018, 14:36
А если иначе, т.е. силы притяжения есть, но они много слабее сил отталкивания?
Что, и такая версия для Вас неприемлема?
А этот вопрос даже всевышнему глупо задавать.
Вы хотели чтобы при единой температуре было всё жидким?
Не надо свои глупости выдавать за мои.
У меня по ТТЭ если это и произойдёт, то только при абсолютно установившейся, т.е. абсолютно постоянной температуре. Чего никак у нас быть не может.
Видимо, в том-то и дело, что Ваша физика - это результат видЕний, а не анализа экспериментальных фактов.
А видЕния, как известно, возникают в мозгу либо в болезненном состоянии, либо под воздействием галюциногенов.
Ешё раз! Не путайте свои видения с моими.
Автор: Digger 20.11.2018, 15:07
Что, и такая версия для Вас неприемлема?
Ну и как в таком случае Вы объясните, что для разрыва воды нужно прложить усилие сравнимое по величине с усилием разрыва сосновой древесины?
Вы хотели чтобы при единой температуре было всё жидким?
Я не писал "при единой температуре", я писал "при данной температуре".
Глупо поминать Всевышнего, не сумев ответить, на простой вопрос о том, почему жидкость при отсутствии сил притяжения, либо их малости по прелестнению с силами отталкивания, не превращается в газ?
У меня по ТТЭ если это и произойдёт, то только при абсолютно установившейся, т.е. абсолютно постоянной температуре. Чего никак у нас быть не может.
Если вы тут о силах сорбции и т.д., то я это весьма чётко объясняю. А Вы по МКТ?
Так ведь, глупость-то Ваша ТТЭ,или Вы этого до сих пор не поняли?
У меня факты, а у Вас видЕния.
Автор: ahedron 20.11.2018, 17:20
Варяг опять создал твинка...
Patent
Вы в своём уме? Какие ещё силы гравитации на уровне атомов и молекул. Гравитация это самый слабый вид взаимодействия. Не нужно её тулить во взаимодействие молекул и атомов.
Автор: mechanic 21.11.2018, 5:17
И здесь следует делать оговорку - при данной температуре.
И оговаривать эту температуру.
Потому как и железо можно сделать жидкостью. Смолу признали жидкостью потому, что она за год выпустила одну каплю. При какой температуре всё это происходило осталось тайной. если бы этот опыт ставился не в центральной Европе, а в Африке, то и капель было больше, а если его ставить на крайнем севере, то и за сотню лет можно капли не дождаться.
В данное время мы обычно всё происходящее относим к обычной температуре, которая нас окружает.
Если тело не теряет свою форму, то его следует относить к твёрдым телам. Но, тогда твёрдые тела следует далее делить по прочностным качествам.
Мягкое, твёрдое, очень твёрдое и т.д.
И если тело начинает течь под действием дополнительной к гравитации силе, то это не должно данное твёрдое тело относить к жидкости.
Вот такое моё мнение.
Здесь уже полное непонимание. Я сейчас не останавливаюсь на объяснении механизма фазового перехода. Он может быть выяснен на микроуровне. А на микроуровне силы гравитации настолько малы, что учитывать их бессмысленно, как, например, в грузоподъемности самосвала вес севшего в кузов комара. Я сейчас говорю совсем не о том. Я говорю о разнице между аморфными и кристаллическими телами на макроуровне. Смолу признали жидкостью прежде всего потому, что у нее, в отличие от железа, нет температуры плавления, а есть диапазон температур, в котором она размягчается до жидкого состояния. У нее нет фазового перехода и скрытой теплоты плавления. Это вы пропутили мимо ушей. Посмотрите на графики фазового перехода из твердого состояния кристаллических тел и аморфных. Это уровень восьмого класса О-о-чень средней школы.
[attachment=257:график_плавления.gif]
При равномерном нагреве, то есть при притоке энергии извне, температура кристаллического тела растет пропорционально притоку тепла на участке АВ, затем, достигнув точки плавления В, она остается неизменной, пока не закончится плавление. После чего на участке ВС температура снова растет прямо пропорционально притоку тепла. Ничего подобного мы не видим на графике плавления аморфного тела. Температура аморфного тела непрерывно возрастает от начальной точки до конечной.
Это очевидные факты и любая теория не будет стоить ломаного гроша, если она неспособна их объяснить. Игнорируя разницу между кристаллическими и аморфными телами ничего путнего создать невозможно.
Откуда взято? Ссылку в студию!
И наконец:
А здесь Вас вдруг потянуло в строение вещества.
Давайте ограничимся наболее общими свойствами веществ с точки зрения механики, чтобы провести чёткую грань между газом, жидкостью и твёрдым телом.
Там где речь идет о термодинамике я говорю о термодинамике, которая является макроскопической наукой, и в ней нет места для теорий строения вещества. Если она ими и пользуется, то только в илюстративных целях. А здесь одним макрроскопическим подходом не обойдешься. Если ограничится только механическим подходом, без температуры, теплоты, и физико-химических процессов, то вообще ни к чему не прийдете, будете толочь воду в ступе.
Автор: Digger 21.11.2018, 7:16
Глава XVIII Физика жидкостей
§ 107. Механические и термодинамические свойства жидкостей
"Прочная капиллярная трубка, запаянная с одного конца, была наполнена водой при 28°, охлаждена до 18°, чтобы в неё вошёл маленький пузырёк воздуха, и запаяна с открытого конца. При повышении температуры, сопровождающемся увеличением давления, воздух растворился в воде. Трубка оказалась целиком наполненной водой. При новом охлаждении до 18° вода продолжала наполнять всю трубку и, следовательно, подверглась всестороннему растяжению. Очевидно, что относительная деформация в данном случае была равна объему существовавшего ранее пузырька воздуха, разделённому на объём воды. Зная модуль объёмной упругости воды, можно было вычислить напряжение, существовавшее в воде. Продолжая охлаждение дальше и доводя воду в трубке до разрыва, представилось возможным определить прочность воды на разрыв. Она оказалась порядка 50 кГ/см2, т. е. всего в 12 раз меньше прочности на разрыв соснового дерева".
К. А. Путилов, Курс физики, том I, МОСКВА 1954
Там где речь идет о термодинамике я говорю о термодинамике, которая является макроскопической наукой, и в ней нет места для теорий строения вещества. Если она ими и пользуется, то только в илюстративных целях. А здесь одним макрроскопическим подходом не обойдешься. Если ограничится только механическим подходом, без температуры, теплоты, и физико-химических процессов, то вообще ни к чему не прийдете, будете толочь воду в ступе.
Причём здесь термодинамика?
Речь идёт о МЕХАНИЧЕСКИХ свойствах вееществ!
Покуда не приведёте определений понятий "газ", "жидкость", "твёрдое тело", которые считаете правильными, до тех пор сия дискуссия будет переливанием из "пустого в порожнее".
Автор: ahedron 21.11.2018, 12:33
Прочность жидкости на разрыв "весьма чистой" воды составляет 100-200 кГ/см2, теоретически 1600 кГ/см2
http://chem21.info/page/219055003152233008241209054193004238071020177214/
Автор: Patent 22.11.2018, 7:28
Не мешайте всё в одну кучу. Я ответил по вопросу чсто с газом.
Если вы его приняли, то оставьте этот вопрос и мой ответ на него в покое.
Не лепите к ответу на вопрос по газу вопрос по жидкости.
А над примером с разрывом воды я подумаю.
А «при данной температуре» разве не означает, что она постоянная?
Что Вы хотите прикрыть этой глупой отмазкой
У меня процесс перехода жидкости в газ рассматривается на уровне поведения отдельных атомов.
Ссылки я давал. Не желаете с ними знакомится – не надо.
Вы здесь даже не знаете, что отнесли к глупости.
Ну да! У Вас и факты про то, что электроны носятся по орбитам вокруг ядра атома и каким-то чудодейственным механизмом участвуют к крепких связях в молекулы.
Вы в своём уме? Какие ещё силы гравитации на уровне атомов и молекул. Гравитация это самый слабый вид взаимодействия. Не нужно её тулить во взаимодействие молекул и атомов.
У меня сильное взаимодействие, слабое взаимодействие и силы гравитации имеют одну природу! У современной физики согласно бритве Оккама здесь две лишние сущности.
Более того, силы смачивания тоже той же природы. Вы верите, что силы смачивания имеют электрическую природу между электрически нейтральными молекулами? Верьте! И это есть Ваша ВЕРА.
Этой же природы силы сорбции и т.п.
А далее в ещё более ослабленном виде проявляются силы гравитации.
Вы знаете природу сильного и слабого взаимодействия?
Я не спрашиваю между чем и чем это взаимодействие. Я спрашиваю про природу сил этого взаимодействия.
Здесь https://d.radikal.ru/d22/1811/56/66b0c1426c10.jpg
на рисунке представлено по ТТЭ соединение трех атомов.

ЭТ – это элементы теплоты. Те, которые участвуют в связи между электронами и ядром обозначены как ЭТ связи. Внутри ядра. Электронов и даже их составляющих также прусутствует множество ЭТ.Часть из них можно отнести к тем, точнее к тому, что считается сильным взаимодействием. То есть, когда ЭТ соединяют нуклоны и т.п. то они организуют сильное взаимодействие. Чем больше соединяется элементов воедино, тем в меньшей мере может проявляться разница между действием суммарных сил притяжения и отталкивания.
Поскольку, например, атомы и молекулы воды и стекла имеют повышенные силы притяжения над силами отталкивания, то проявляется явление смачиваемости. А если нет, то проявляется НЕсмачивание.
Жду этого выяснения.
Я вообще о конкретной температуре размягчения смолы не говорил.
А если её держать на кайнем севере и она так и не выпустит ни одной капли, то как к этому следует относится? Признать её в этом дапазоне температур жидкостью или нет?
См. на это ответ выше.
Автор: Digger 22.11.2018, 7:40
Как обычно приписываете оппоненту, то чего он никогда не говорил.
У меня нет ни малейшего желания продолжать беседу с чловеком, который ради пропаганды своих безумных теорий, приписывает оппоненту глупости.
Конец связи.
Автор: mechanic 22.11.2018, 8:17
Справочник химика...
Обратите внимание, речь идет не об обычной воде, встречаемой в природе, и содержащей механические примеси, растворенный в воде воздух и минеральные соли. Это все относится к специально подготовленной воде. Кстати, кроме сопротивления разрыву и сжатию вода может испытывать деформации сдвига, а им она сопротивляется очень слабо, по крайней мере природная вода. И еще один важный момент. Если пройти по ссылке на справочник химика, то на стр. 77. можно прочесть немаловажную информацию:
Это как раз то, о чем я говорил: агрегатное состояние вещества зависит не только от температуры, но и от давления.
Речь идёт о МЕХАНИЧЕСКИХ свойствах вееществ!
Покуда не приведёте определений понятий "газ", "жидкость", "твёрдое тело", которые считаете правильными, до тех пор сия дискуссия будет переливанием из "пустого в порожнее".
Так это же вы сами предъявили мне претензию, что когда я говорил о термодинамике, то не касался молекулярной теории строения вещества. И я вам объяснил, что темодинамика макроскопическая наука, не основанная на гипотезах строения вещества. А сейчас мы занимаемся агрегатными состояниями вещества. Этим занимается и механика и физическая химия, и термодинамика. У каждой из этих наук свой подход и свои методы исследования, а также свои определения понятий. С точки зрения механики твердое тело это тело, сохраняющее свою форму. Поэтому к твердым телам с этой точки зрения относят и кристаллические и аморфные тела. Термодинамический подход исследует зависимость агрегатного состояния вещества от внутренней энергии тела как термодинамической системы. При этом выясняется, что аморфные вещества ведут себя совершенно иным способом нежели кристаллические. При фазовом переходе плавление - затвердевание отсутствует энергетический барьер между жидкостью и твердым телом, то есть аморфное тело ведет себя как жидкость. Физическая химия исследует строение вещества и выясняет, что истинно твердые тела с точки зрения термодинамики это тела, имеющие кристаллическую решетку, для разрушения которой необходимо подвести к телу скрытую теплоту плавления. При обратном процессе - кристаллизации, эта энергия выделяется. Аморфные тела имеют молекулярную структуру, аналогичную вязкой жидкости.
Автор: Digger 22.11.2018, 8:48
Неужели Вы не понимаете, что до тех пор, покуда не договоримся об определениях агрегатных состояний (что называть газом, жидкостью, или твёрдым телом), до тех пор наша дискуссия бессмысленна?!
Я неоднократно обращался к Вам с просьбой привести определения этих понятий, которые считаете правильными, но так их и не услышал.
Поэтому прододжение дискуссии без договоренности об определения этих понятий считаю пустой тратой времени.
Автор: Patent 22.11.2018, 9:47
У меня нет ни малейшего желания продолжать беседу с чловеком, который ради пропаганды своих безумных теорий, приписывает оппоненту глупости.
Так Вы разве не поддерживаете полёты электронов вокруг ядер атомов?
Не возражаю.
Это в первую очередь касается перехода из одного агрегатного состояния в другое.
И я это вполне внятно могу объяснить на уровне поведения атомов. А вы?
Автор: ahedron 22.11.2018, 12:33
Patent
То есть: хочу будет сильным гравитационное взаимодействие, а захочу - будет слабым... ну чистой воды сказочник. Природа у всего одна, нету двух разных Природ!!!
Кстати, на вашем рисунке, что за соединение получилось из трёх атомов и какими свойствами оно обладает и почему именно эта молекула, а не, допустим, молекула воды - тоже из трёх атомов. Или вы так, от балды нарисовали и суёте это всем под нос, говоря, что это ваша гипотеза?
Автор: Patent 22.11.2018, 12:59
То есть: хочу будет сильным гравитационное взаимодействие, а захочу - будет слабым... ну чистой воды сказочник. Природа у всего одна, нету двух разных Природ!!!
Кстати, на вашем рисунке, что за соединение получилось из трёх атомов и какими свойствами оно обладает и почему именно эта молекула, а не, допустим, молекула воды - тоже из трёх атомов. Или вы так, от балды нарисовали и суёте это всем под нос, говоря, что это ваша гипотеза?
По раскладу сил (!) от моего хочу ничего не зависит.
А Вы как раньше эмоциями вместо аргументов размахивали, так хотите и дальше.
Запретить не могу.
Автор: ahedron 22.11.2018, 15:55
Patent, Вы не ответили ни на один мой вопрос, а только махаете над головой своими несуществующими шариками. Я пытаюсь вас вылечить, но по ходу: пациент не поддаётся лечению.
Автор: Patent 22.11.2018, 18:45
Я и в предыдущем посте дал внятный ответ на вопрос-эмоцию
А здесь я дал достаточно детальный ответ в сопровождении с графикой.
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164079
Если мои ответы не согласуются с Вашим ожиданием, то это не значит, что я их не давал.
Что-то вы забываете про электроны, которые в Вашей голове (и не только в вашей) как ужаленные шарики летают в отдалении от ядра атома.
Что-то я не видел от Вас причин по которым они не падают на ядро. А самое главное, что-то Вы никак не можете объяснить - как атомы с этими летающими с околосветовой скоростью шариками соединяются в молекулы и образуют прочные связи.
А у меня всё это представлено просто и внятно.
Автор: ahedron 22.11.2018, 21:18
Patent, Перестаньте приписывать другим то, о чём они и в помине не говорили. Вам уже не раз это было сказано.
Внятно для кого? Только для вас.
Автор: Patent 23.11.2018, 20:48
Повторяю и для Вас. Если Вы поддерживаете основы МКТ, то этим поддерживаете полёты электронов вокруг ядра атомов.
Это исходя из МКТ их наградили энергией в виде кинетической.
А значит должны иметь объяснения того, как при этих обстоятельствах атомы образуют прочные связи.
У Вас это есть?
Для тех, кто в ТТЭ вникает.
Мне в личку многие пишут слова благодарности.
Автор: mechanic 24.11.2018, 7:12
Я неоднократно обращался к Вам с просьбой привести определения этих понятий, которые считаете правильными, но так их и не услышал.
Поэтому прододжение дискуссии без договоренности об определения этих понятий считаю пустой тратой времени.
От того, что мы здесь договоримся, дискуссия осмысленной не станет. Мы сейчас договоримся считать кошку собакой, а она все равно не научится лаять.Вы не пытаетесь вникнуть в суть проблемы, а хотите чтобы вам преподнесли определения на блюдечке с голубой каемочкой. А почему сами не сформулируете, хотя бы из того, что я написал о твердом состоянии вещества? Вы, как я понимаю, придерживаетесь самой примитивной, совпадающей с бытовой трактовки агрегатных состояний вещества. Это соответствует механическому взгляду на проблему. Газ, например, не имеет ни формы, ни объема; жидкость имеет объем , но не имеет формы и принимает форму сосуда, а в невесомости при наличии атмосферного давления принимает форму шара; твердое состояние вещества характеризуется сохранением объема и формы. Если вас такие определения вполне устраивают, то меня -- нет, и мы ни о чем не договоримся.
Дело в том, что есть и другой. также макроскопический взгляд на эту проблему, а именно, энергетический (термодинамический). Известен опыт, при котором вы никогда не сможете на водяной бане вскпятить воду. Довести до температуры кипения - да, а вскипятить - никогда!, если , конечно не изменить условия опыта, напрмер, подсолив воду во внешней емкости. Почему так происходит? Дело в том, что для того, чтобы превратить в пар 1 кг воды при 100⁰С необходимо затратить 539 ккал теплоты без повышения температуры. Иными словами, внутренняя энергия 1кг пара при 100⁰С, больше внутренней энергии воды при 100⁰С на 539 ккал. Этот энергетический барьер называется скрытой теплотой парообрпзования.
Аналогично, при 0⁰С между льдом и водой при 0⁰С существует энергетический барьер в 80 ккал/кг. Он называется скрытой теплотой плавления. Все было бы хорошо, если бы не было так плохо. Оказывается что не все твердые, по мнению механиков, вещества имеют энергетический барьер. Этому правилу подчиняются только кристаллические вещества. А вот аморфное хулиганье не соблюдает правила поведения. Аморфные вещества не только не обладают скрытой теплотой плавления, но и не имеют определенной температуры плавления. Поэтому с точки зрения термодинамики истинно твердыми телами называются кристаллические тела, а аморфные представляют собой вязкие жидкости.
Спор между "механиками" и "термодинамиками" должна решить физическая химия, которая копает глубже - в мир строения вещества на уровне атомов и молекул. Но у нее мы спросим в следующий раз.
Автор: Digger 24.11.2018, 8:53
Вот это и называется шулерство:поскольку Вы предлагаете называть собакой то, что мяукает (стекло жидкостью).
Всего делов-то: договориться что называть "кошкой", а что "собакой".
Но Вы этого упорно не желаете делать, видимо, прекрасно понимая, что ни в какой физхимии, ни в химфизике нет чёткого определения понятий "газ", "жидкость" и "твёрдое тело".
Поскольку если бы они были, то Вы бы давно их озвучили.
Ещё раз привожу определения понятий "газ", "жидкость" и "твёрдое тело", которые общеприняты, и которые я считаю правильными:
"Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом), агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь предоставленный им объём".
(БСЭ)
"Жидкость, агрегатное состояние вещества, промежуточное между твёрдым и газообразным состояниями. Ж., сохраняя отдельные черты как твёрдого тела, так и газа, обладает, однако, рядом только ей присущих особенностей, из которых наиболее характерная — текучесть. Подобно твёрдому телу, Ж. сохраняет свой объём, имеет свободную поверхность, обладает определённой прочностью на разрыв при всестороннем растяжении и т. д. С другой стороны, взятая в достаточном количестве Ж. принимает форму сосуда, в котором находится".
(БСЭ)
"Твёрдое тело, одно из четырёх агрегатных состояний вещества, отличающееся от др. агрегатных состояний (жидкости, газов, плазмы) стабильностью формы и характером теплового движения атомов, совершающих малые колебания около положений равновесия. Наряду с кристаллическим состоянием Т. т. (см. Кристаллы) существует аморфное состояние, в том числе стеклообразное состояние".
(БСЭ)
Аналогично, при 0⁰С между льдом и водой при 0⁰С существует энергетический барьер в 80 ккал/кг. Он называется скрытой теплотой плавления. Все было бы хорошо, если бы не было так плохо. Оказывается что не все твердые, по мнению механиков, вещества имеют энергетический барьер. Этому правилу подчиняются только кристаллические вещества. А вот аморфное хулиганье не соблюдает правила поведения. Аморфные вещества не только не обладают скрытой теплотой плавления, но и не имеют определенной температуры плавления. Поэтому с точки зрения термодинамики истинно твердыми телами называются кристаллические тела, а аморфные представляют собой вязкие жидкости.
Спор между "механиками" и "термодинамиками" должна решить физическая химия, которая копает глубже - в мир строения вещества на уровне атомов и молекул. Но у нее мы спросим в следующий раз.
Хватить юлить и выкручиваться!
Приведите определения понятий "газ", "жидкость" и "твёрдое тело", которые считаете правильными, хоть механическое, хоть физхимическое, хоть термодинамическое.
Автор: зайсаСан 24.11.2018, 13:34
Шкурный вопрос дилетанта ....
Возможно ли действие кавитации на преобразование вещества ?
К примеру , - возможно ли "переделка" кислорода в углерод?
Не будет ли такое преобразование пощёлкивать ?!
По молекулярному весу кислород - 16 , углерод - 12 ...т.е. отрываем 4-е электрона с внешней орбиты кислорода ...
Хобби у меня такое - искать необьяснённое ... ;-)
Сейчас под вопросом "горючее по Краснову Ю. "
Автор: Digger 24.11.2018, 14:28
По молекулярному весу кислород - 16 , углерод - 12 ...т.е. отрываем 4-е электрона с внешней орбиты кислорода ...
Хобби у меня такое - искать необьяснённое ... ;-)
Сейчас под вопросом "горючее по Краснову Ю. "
И этим всё сказано!
Оторвав 4 электрона у атома кислорода, получим тот же атом кислорода с массой 16 а.е.м., но только ионизированный.
Для справки:
(масса электрона почти в 2000 раз меньше массы протона или нейтрона)
Вам бы, любезный, азы выучить, а уж потом поднимать шкурные вопросы.
Автор: vps137 24.11.2018, 15:10
Приведите определения понятий "газ", "жидкость" и "твёрдое тело", которые считаете правильными, хоть механическое, хоть физхимическое, хоть термодинамическое.
Интересно, что вы такое собираетесь делать с этими определениями?
Автор: Digger 24.11.2018, 15:44
Знание определений не оставляет места для жульничества и фантазий.
Но Вам-то, фантазёру, определения ни к чему.
Не так ли?
Автор: зайсаСан 24.11.2018, 17:20
Оторвав 4 электрона у атома кислорода, получим тот же атом кислорода с массой 16 а.е.м., но только ионизированный.
Для справки:
(масса электрона почти в 2000 раз меньше массы протона или нейтрона)
Вам бы, любезный, азы выучить, а уж потом поднимать шкурные вопросы.
Поздновато мне уже начинать с азов....да и не химик я ....
Обьясняю ситуёвину:
При приготовлении горючего по Краснову применяется ультразвук в виде свистка . В контуре обмена воды присутствует завихритель , холодильник , насос высокого давления для работы УЗ свистка.
Получаемая эмульсия по словам автора , на расслаивается до 3-4 месяцев .
Но дело не в этом эффекте .
Использование такого состава (по уверениям автора)имеет применение в горелках и в транспорте .
Я провёл испытания по получению эмульсии и выяснилось , что эмульсия в пределах 5% достаточно устойчивая в течении суток . Эмульсия в пределах 10% уже даёт чёткую картинку образования эмульсионных шариков т.е. для реакции в реакторе годится, но расслаивание идёт более активно .
Краснов в своей публикации писал о неких добавках, но они влияют только на растворимость вещества в веществе . Мной применялась очищенная вода ,близкая по свойствам к дистилляту.
Если поразмышлять насчёт горючести то сама по себе вода не будет гореть до создания особых условий.
Особые условия это раскалённый пар в контакте с железом- образование водорода + кислород и + расход собственно самого железа .
Кста , по моему это и является грандиозным пожаром в Калифорнии (куча железок(автомобилей , почтовых ящиков,декоративных вывесок и т.п. ) с бензином явились катализатором пожара)
Но в установке Краснова получают только обработанную воду которая , кста, по уверениям самого автора - горит!
Отсюда :
В реакции должен учавствовать углерод ..но откуда,ж ему взяться ? Та часть что подмешана в воду ,совсем мизерна и будет гореть в самом начале процесса .
Нагрев же эмульсии приведйёт к значительному разряжению горючего и к получению в лучшем случае смеси метана с паром(водой)
Т.е. метан то получен , но увы ,,,количество горючки не изменилось .
Отсюда и вопрос ,- возможно ли переделать кислород в углерод столь простым способом ?
;-)
Я нашёл ещё одну публикацию ,но там автор приводит в качестве катализатора железную сетку и утверждает , что металл не расходуется на получение водорода .
???
Странно ! Ведь для хим/реакций требуется промежуточная реакция для закрепления предыдущей.
К примеру :
Разложение высокой температурой воды не даст водород и кислород в отдельности , да и в куче тоже не даст ...требуется "фиксатор" в виде тогоже железа т.е. в реакции горит также и железо(ФеО) . По простым расчётам на 1литр воды требуется 3кг железа .....грустновато....
Автор утверждает , что в качестве катализатора учавствует именно эта мизерная добавка углеводородного топлива ....возможно ли это ?
Автор: Digger 24.11.2018, 18:07
Обьясняю ситуёвину: [...............]
На вашем месте я бы начал с попытки понять как работает катализатор.
Как вещество ускоряющее течение химической реакции, и при этом не расходуемое, эту самую реакцию ускоряет?!
На этот вопрос я долго искал ответ в учебниках, но, увы-с...
Например платина, палладий, рутений (металлы платиновой группы) используются в качестве катализаторов во многих химических производствах.
А без азов от хобби Вашего проку, как от ..... молока.
Конец связи.
Автор: зайсаСан 24.11.2018, 19:18
А без азов от хобби Вашего проку, как от ..... молока.
Конец связи.
НУ что вы в самом деле ...я же не претендую на глобальные знания .
Когдато я обратлся по поводу получения горючки к одному химику . Оказалось , что он живёт в моём раёне, но оказалось , что он давно помер и на разговор вышел его сын ...тоже химик . Поразило то , что обьеденяет химиков какаято мантра . Т.е. обьяснить элементарное им вера не велит!
У меня по химии была твёрдая пятёрка в школе . Сейчас подзабыл уже ...осталось - "калий,натрий,серебро -одновалентное добро" ;-) ну и несколько опытов с гремучкой , золотом, ....
Наиболее продуктивным был крекинг бензина , получение сгущёнми , получение горючки из пластмассы (это уже в домашних условиях)....
Ну вам то это неинтересно... обычные температурные пороги.
Сейчас мне интересно получение горючки по Краснову Ю. Пока все показания сходятся на негативе ...увы....вот я и ищу либо свою ошибку , либо заблуждения Краснова.
Возможно в ветке появится кто нить с продолжением тематики ??!
Основа - эмульсия на бумаге ведёт себя также как и на жестяной полоске т.е. не горит нифига (пыхает) . Но пыханье - это реакция креринга в результате чего образуется метан - он то и пыхает ....
Автор: vps137 24.11.2018, 19:42
Но Вам-то, фантазёру, определения ни к чему.
Не так ли?
Нет, что вы! Меня интересуют определения, но только в другоой области. Да, она кажется фантастической. Я считаю, ну и пусть - лишь бы результат был.
Но вы не ответили - зачем вам?
Автор: Digger 24.11.2018, 20:53
Но вы не ответили - зачем вам?
Результат - это, что, по вашему?
Что касается того, зачем мне определения, то ответ прост: чтобы не запутаться самому и не быть запутанным другими, когда пытаешься понять устройство Мира.
Нет определений - нет чётко обозначенных договоренностей об одинаковом понимании вещей. Нет договоренностей - нет и не может быть конструктивного диалога.
Результат отсутствия взаимопонимания - Вавилонское столпотворение.
Автор: alal 25.11.2018, 13:07
В каком фазовом состоянии вот это ?
https://youtu.be/YlQKG4TIoIU?t=30
![]()
Автор: Digger 25.11.2018, 14:59
https://youtu.be/YlQKG4TIoIU?t=30
При быстром изменении приложенных сил - твёрдое тело, а при медленном жидкость.
Автор: mechanic 26.11.2018, 7:28
В каком фазовом состоянии вот это ?
Какая фаза ?
rolleyes.gif
При быстром изменении приложенных сил - твёрдое тело, а при медленном жидкость.
Наконец-то! Здравый смысл начинает пробивать дорогу.
alal, замечательный пример против косности и застоя. Поставил бы два плюса. но некуда. Вот чего стоят односторонниеи неполные определения из БСЭ, учитывающие только механическую точку зрения, но даже и она подверглась позорному разгрому. Оказывается появляется дуализм: при одной и той же температуре аморфное тело проявляет то свойство твердого тела, то жидкого. Все зависит от скорости приложения силы. Представьте себе на минуту, если бы Крымский мост был бы сделан из такого материала. Когда автомобили быстро пересекают мост он сохраняет свою прочность как твердое тело. Но тут затор - заглох мотор и мост со всеми находящимися на нем транспортными средствами начинает стекать в Азовское море. К счастью, кроме аморфных тел, которые рядятся в твердые тела, есть и истинно твердые - кристаллические тела, прочность которых при заданной температуре не зависит от скорости приложения нагрузки, а только от ее величины. Все это: и механические, и термодинамические свойства твердых тел. говорят о том, что к определению твердого тела надо подходить с различных позиций, а физико -химическое строение вещества подтверждает это предположение. Почитайте страницы из хорошо известного учебника Глинки "Общая химия".
[attachment=258:p0179.png] [attachment=259:p0180.png] [attachment=260:p0181.png]
Обратите особое внимание на последний абзац перед гл.VI:
Вследствие сходства во внутренней структуре жидкостей и аморфных тел последние часто рассматриваются как жидкости с очень высокой вязкостью, а к твердым телам относят только вещества в кристаллическом состоянии..
Вот поэтому и стеклянный бокал можно смело назвать жидкостью. Отмечу еще одну немаловажную деталь. Ряд аморфных тел с течением времени переходят в кристаллическую форму. Примерами могут служить засахаривание меда, помутнение старинных стекол и т.д. Обратного перехода не бывает никогда. Это процесс необратимый, и, в соответствии со вторым началом термодинамики, кристаллическая структура должна иметь меньший уровень внутренней энергии, чем аморфные. Аморфные тела образуются тогда, когда процесс увеличения вязкости при охлаждении жидкости опережает процесс кристаллизации. Аморфные тела можно рассматривать как переохлажденные жидкости высокой вязкости. А, как известно, переохлажденные жидкости являются , в принципе, неустойчивыми структурами.
Теперь обратимся к газообразному состоянию вещества.
"Газы (французское gaz; название предложено голланским учёным Я. Б. Гельмонтом), агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно, заполняя весь предоставленный им объём".
(БСЭ)
К этому определению также есть претензии. Исторически газами называли "несжижаемые газы", а сжижаемые газы относили к парАм. С развитием криогенной техники все газы удалось перевести в жидкое состояние, но различие между паром и газом осталось. Газы при нормальных условиях весьма хорошо подчиняются газовым законам, объединенным в уравнение Клапейрона -Менделеева. Пары - допускают отклонения от этого уравнения и тем большие, чем ближе пар находится к точке конденсации. А насыщенные пары вообще не подчиняются газовым законам.
Определение данное в БСЭ не заостряет внимания на это принципиальное различие между паром и газом, отделываясь расплывчивым выражением "частицы не связаны или весьма слабо связаны силами взаимодействия".
На самом деле, газами должны называться разреженные (перегретые) пары, в которых размерами частиц и силами взаимодействия между ними можно пренебречь в виду их малости. Такое состояние хорошо описывается молекулярно -кинетической теорией, которая позволила теоретически вывести законы идеальных газов, ранее выведенные экспериментально для газов при нормальных и близких к ним условиях. Как известно, законы идеальных газов являются приближенными. Отступления реальных газов от них носят как количественный, так и качественный характер. Количественные отступления проявляются в том, что уравнение Клапейрона PV=RT для реальных газов соблюдается приближенно, а качественные отступления - более серьезны. Если бы реальные газы подчинялись уравнению Клапейрона, то их было бы невозможно перевести в жидкое и твердое состояния. О причинах этих отступлений мы поговорим в дальнейшем.
Теперь отвечу зайсаСану. Тот вопрос, который вас интересует не относится к данной теме. Поговорим в теме Термодинамика позднее.
Автор: Digger 26.11.2018, 7:42
Хватит болтать ерундой!
Здравый смысл появится только тогда, когда договоримся об определениях понятий "газ", "жидкость" и "твёрдое тело".
Нет определений - нет предмета обсуждения.
Фсё!
Автор: alal 26.11.2018, 11:56
Здравый смысл появится только тогда, когда договоримся об определениях понятий "газ", "жидкость" и "твёрдое тело".
Нет определений - нет предмета обсуждения.
Фсё!
Digger,
вы поймите, определения имеют значение в единственной области деятельности человечьего ума - в математике, потому что она никак не связана с внешним миром
Даже такая умозрительня и существующая только при наличии человеков область как юриспруденция допускает ТОЛКОВАНИЯ определений, за счет чего и жуют хлеб с икрой толкователи-юристы, судьи, адвокаты
В физике определения также расплывчаты и неопределенны как и любые суждения человеков о внешнем мире.
Чего стоит ваше извлечение из БСЭ:
"агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно"
Что такое "весьма слабо", что такое " движутся свободно" ?
Это из поэзии, медицины, декларации прав человека ?
Тут уже много раз сказано - все человечьи определения заканчиваются ссылкой на неопределямого Первопричинника.
Автор: ahedron 26.11.2018, 12:10
Давайте на этом и остановимся.
Или сначала ответьте на вопрос: зачем делить тела на агрегатные состояния? Тем более, произносить при определении обязательную фразу:"При нормальных условиях." Кто тут нормальный? В каком месте постоянные нормальные условия?
Автор: Digger 26.11.2018, 13:10
вы поймите, определения имеют значение в единственной области деятельности человечьего ума - в математике, потому что она никак не связана с внешним миром
Даже такая умозрительня и существующая только при наличии человеков область как юриспруденция допускает ТОЛКОВАНИЯ определений, за счет чего и жуют хлеб с икрой толкователи-юристы, судьи, адвокаты
В физике определения также расплывчаты и неопределенны как и любые суждения человеков о внешнем мире.
Чего стоит ваше извлечение из БСЭ:
"агрегатное состояние вещества, в котором его частицы не связаны или весьма слабо связаны силами взаимодействия и движутся свободно"
Что такое "весьма слабо", что такое " движутся свободно" ?
Это из поэзии, медицины, декларации прав человека ?
Тут уже много раз сказано - все человечьи определения заканчиваются ссылкой на неопределямого Первопричинника.
Определение понятий - это то с чего начинается наука, поскольку не договорившись о том, какой смысл мы вкладываем в то или иное понятие, мы неизбежно придём к взаимонепониманю.
Можно сколько угодно критиковать существующие и общепринятые определения, ибо почти всё в этом мире со временем устаревает.
Но отказавшись от устаревшего и кажущегося нам неправильным, мы просто обязаны не просто выбрасывать это устаревшее, а заменять его новым и более, на наш взгляд, правильным.
Поэтому-то и нужно договориться о том какой смысл мы вкладываем в определения тех или иных понятий.
Коль Вам не нравится определение из БСЭ, приведите своё определение, которое считаете правильным, и тогда появится предмет обсуждения.
А пока же получается полная анархия: хочу назову жидкостью воду, а хочу стекло.
Хочу керосин, а хочу асфальт.
Для примера приведу своё определение понятия "жидкость", которое считаю правильным:
Жидкость - агрегатное состояние вещества при котором оно может принимать форму сосуда, в котором находится, подчиняется закону сообщающихся сосудов, а в невесомости принимает форму шара.
Вот и давайте договариваться, либо критикуя существующие определения, и давая взамен свои, либо принимать их.
Иного пути нет.
"Нет определений" - нет науки, а есть псевдонаучная болтовня.
А заниматься ею у меня нет ни малейшего желания.
Или сначала ответьте на вопрос: зачем делить тела на агрегатные состояния? Тем более, произносить при определении обязательную фразу:"При нормальных условиях." Кто тут нормальный? В каком месте постоянные нормальные условия?
Ну вот, ещё один, тИАретик, не знающий азов.
Нормальные условия, 1) условия применения средств измерений, при которых влияющие величины (температура, питающее напряжение и др.) имеют нормальные (установленные) значения или находятся в пределах области допускаемых отклонений от этих значений. Н. у. указываются на шкалах средств измерений, в стандартах на них, технических описаниях и инструкциях к использованию. Пределы допускаемых основных погрешностей средств измерений устанавливаются для Н. у. Для электроизмерительных приборов за Н. у. часто принимают следующие: температура — в пределах 20 ± 2 °С, питающее напряжение — указанное на шкале ± 2%, частота — в пределах 49 — 51 гц и т.д. 2) Физические условия, определяемые давлением р = 101325 н/м2 = 760 мм рт. ст. (нормальная атмосфера) и температурой 273,15 К (0 °С), при которых мольный объём идеального газа Vo= 2,24136 · 10-2 м3/моль. Нормальное ускорение свободного падения принимают равным gn= 9,80665 м/сек2.
(БСЭ)
Автор: alal 26.11.2018, 14:27
Можно сколько угодно критиковать существующие и общепринятые определения, ибо почти всё в этом мире со временем устаревает.
Но отказавшись от устаревшего и кажущегося нам неправильным, мы просто обязаны не просто выбрасывать это устаревшее, а заменять его новым и более, на наш взгляд, правильным.
Поэтому-то и нужно договориться о том какой смысл мы вкладываем в определения тех или иных понятий.
Коль Вам не нравится определение из БСЭ, приведите своё определение, которое считаете правильным, и тогда появится предмет обсуждения.
А пока же получается полная анархия: хочу назову жидкостью воду, а хочу стекло.
Хочу керосин, а хочу асфальт.
Для примера приведу своё определение понятия "жидкость", которое считаю правильным:
Жидкость - агрегатное состояние вещества при котором оно может принимать форму сосуда, в котором находится, подчиняется закону сообщающихся сосудов, а в невесомости принимает форму шара.
Вот и давайте договариваться, либо критикуя существующие определения, и давая взамен свои, либо принимать их.
Иного пути нет.
"Нет определений" - нет науки, а есть псевдонаучная болтовня.
А заниматься ею у меня нет ни малейшего желания.
Наука начинается и заканчивается измерениями, сравнениями результатов измерений.
Не преувеличивайте роль определений - это удел филологии.
Насыпьте в каструлю песка - примет форму сосуда?
Насыпьте песка в сообщающиеся сосуды и поставьте на вибростенд ?
Кстати, сфера - не физическое понятие, а чисто математическое, ну да ладно.
В невесомости, говорите, - значит любые вещества НЕпобывавшие в невесомости и НЕпринявшие сферическую форму с точностью , ну сколько - 0,000000001%, за сколько - за, допустим одну секунду, НЕ СЧИТАТЬ жидкостью, согласны ?
Вот из клипа hand gum, как думаете протечет сквозь сообщающиеся сосуды, за сколько времени, при какой силе тяжести, а хоть какую-то псевдосферичность приобретет в невесомости, за сколько времени?
Только измерения и сравнения, никакой филологии
Автор: Digger 26.11.2018, 16:00
Не преувеличивайте роль определений - это удел филологии.
Насыпьте в каструлю песка - примет форму сосуда?
Насыпьте песка в сообщающиеся сосуды и поставьте на вибростенд ?
Кстати, сфера - не физическое понятие, а чисто математическое, ну да ладно.
В невесомости, говорите, - значит любые вещества НЕпобывавшие в невесомости и НЕпринявшие сферическую форму с точностью , ну сколько - 0,000000001%, за сколько - за, допустим одну секунду, НЕ СЧИТАТЬ жидкостью, согласны ?
Вот из клипа hand gum, как думаете протечет сквозь сообщающиеся сосуды, за сколько времени, при какой силе тяжести, а хоть какую-то псевдосферичность приобретет в невесомости, за сколько времени?
Только измерения и сравнения, никакой филологии
Чтобы что-то измерить, этому измеряемому необходимо дать определение.
Например, скорость - расстояние проходимое телом а единицу времени.
Математикам с их абстрактным мышлением, для которых число и есть объективная реальность, всё, что не может быть записано числом - филология.
Не лезьте вы в физику, т.к. физика, отнюдь, не математика.
Конец связи.
Автор: alal 26.11.2018, 16:07
Например, скорость - расстояние проходимое телом а единицу времени.
Математикам с их абстрактным мышлением, для которых число и есть объективная реальность, всё, что не может быть записано числом - филология.
Не лезьте вы в физику, т.к. физика, отнюдь, не математика.
Конец связи.
Ну если вы такой ФИЗИК, то не используйте математических понятий в физических определениях.
А представляете, где бы мы до сих пор были, если бы Фарадей, Герц, Кюри ждали от филологов определений , а не занимались бы измерениями, физикой, не было на тот момент определений того, что они открыли
Автор: mechanic 27.11.2018, 4:11
Или сначала ответьте на вопрос: зачем делить тела на агрегатные состояния? Тем более, произносить при определении обязательную фразу:"При нормальных условиях." Кто тут нормальный? В каком месте постоянные нормальные условия?
Давайте не будем здесь "ахедронить", если можно так выразиться. Digger привел верные определения так называемых нормальных условий. Для всякого рода измерений необходимо условиться о каких- то точках отсчета. Например, земной шар расчертили координатной сеткой: параллелями и меридианами. Гринвичкий меридиан условились считать нулевым. От него , в частности, отсчитываются часовые пояса. Стандартным ускорением силы тяжести принято ускорение силы тяжести на широте Парижа, а за точку отсчета атмосферного давления - давление на уровне моря (760 мм. рт. ст.) и т.д. и т.п. Это международные стандарты, необходимые для обеспечения единства измерений, а не психушка, где выясняют, кто нормальный, а кто нет.
Никто не делит тела на агрегатные состояния. Любое химически стойкое тело может находиться в любом агрегатном состоянии в зависимости от условий , в которых оно находится. Это такой же неоспоримый факт, как у кошки четыре ноги - один хвост. Но такое определение кошки является неполным и явно недостаточным, чтобы отличить ее от собаки или коровы. Можно конечно добавить: "но трогать ее не моги за ее малый рост" и т.д. Но есть на кошку и другая точка зрения. С точки зрения мыши это самый страшный зверь. Вот так дело обстоит с определениями, если они не являются сугубо абстрактными. Например, идеальные газы это газы, строго подчиняющиеся уравнению Клапейрона . И никаких гвоздей! Можно определять понятия не какой- нибудь одной формулировкой, а набором признаков и свойств, имеющих отношение к изучаемой проблеме. Вот я и пытаюсь это сделать, особенно в тех случаях, когда в различных источниках рассматривается проблема с различных точек зрения. Я уже приводил определения твердого тела с точки зрения механики, термодинамики , физической химии. А вот какое мнение о твердом состоянии вещества высказано в одном из лучших курсов - Элементарный учебник физики под ред. Ландсберга .
[attachment=261:p0509__2_.jpg] [attachment=262:p0510__2_.jpg]
Здесь я хотел бы выделить фразу на втором изображении: "при затвердевании аморфных веществ не происходит перехода вещества в новое состояние" О чем это говорит? Если это была жидкость, то после затвердевания она и осталась жидкостью! И далее:" Затвердевание смолы или стекла - только постепенное загустевание их. Стекло можно рассматривать как очень густую жидкость.
Может быть Digger наконец- то убедился, что истинно твердыми телами можно называть только кристаллические тела.
Вы можете спросить какое это имеет значение? Ответ: Принципиальное. В аморфных телах силы притяжения и отталкивания между частицами действуют как и в жидкостях, а в кристаллических телах - как в истинно твердом теле.
Автор: vps137 27.11.2018, 7:49
Можно лишь дополнить в Вашем сообщении то, что переход при затвержевании в аморфном состоянии является фазовым переходом второго рода. При нём не происходит выделение или поглащение энергии, как при переходах первого рода, а идёт изменение симметрии, что соправождается ростом теплоёмкости по закону [imath]|T_C-T|^{\alpha}[/imath] . Для перехода в стекло показатель альфа равен 0.59. (https://en.wikipedia.org/wiki/Phase_transition#Critical_exponents_and_universality_classes)
Автор: Digger 27.11.2018, 8:08
Вы можете спросить какое это имеет значение? Ответ: Принципиальное. В аморфных телах силы притяжения и отталкивания между частицами действуют как и в жидкостях, а в кристаллических телах - как в истинно твердом теле.
А вот с этого места поподробнее:
Считается, что все металлы имеют кристаллическое строение.
Разве капля расплавленного металла не принимает шарообразную форму?
Какие силы, если не силы притяжения заставляют каплю расплпавленого металла принимать шарообразную форму?
Автор: ahedron 27.11.2018, 12:12
Я о чём... а не о том что вы тут понаписали.
Полетели мы изучать космос, относительно каких нормальных условий вы будете определять свойства веществ... относительно широты Парижа? Мде.
Водород становится металлом... при определённых условиях, поэтому ваши нормальные условия - в топку, если вы только не думаете, что человечество всю жизнь проведёт на Земле, а вы в своих норках.
Автор: mechanic 27.11.2018, 19:08
Считается, что все металлы имеют кристаллическое строение.
Разве капля расплавленного металла не принимает шарообразную форму?
Какие силы, если не силы притяжения заставляют каплю расплпавленого металла принимать шарообразную форму?
А где вы прочли обратное? Все без исключения жидкости стремятся принять шарообразную форму в отсутствии других сил препятствующих сему. Вопрос только в природе и механизме действия этих сил. Единственно. что можно сразу отмести - это действие гравитационных сил в качестве указанных вами сил притяжения в виду их ничтожности. Яркими примерами, шарообразной формы жидкости являются шарики ртути на стекле, дереве, то есть на несмачиваемых поверхностях, капли дождя в воздухе также имеют шарообразную форму. А на смачиваемых поверхностях капли ртути и воды растекаются под действием других сил.
А в чем вопрос-то? Все чистые металлы действительно имеют кристаллическое строение в твердой фазе, а в жидкой, разумеется, нет. При чем тут шарообразная форма? И еще: не СЧИТАЕТСЯ, что металлы имеют кристаллическое строение, а НАБЛЮДАЕТСЯ невооруженным глазом, в лупу или в микроскоп.
Полетели мы изучать космос, относительно каких нормальных условий вы будете определять свойства веществ... относительно широты Парижа? Мде.
Водород становится металлом... при определённых условиях, поэтому ваши нормальные условия - в топку, если вы только не думаете, что человечество всю жизнь проведёт на Земле, а вы в своих норках.
Вот это называется пустой болтовней. Свойства веществ не зависят от выбора системы координат. А вот вес тел зависит. Поэтому и дается привязка к Парижскому меридиану, где хранится эталон килограмма. В космосе она не нужна. В своей квартире вам не нужно измерять расстояния от нулевого меридиана, можно измерять от печки или от фонаря.
Состояние веществ зависит, например, от температуры, давленияи и т.д. Для их измерения надо выбрать и единицы измерения и точки отсчета, совокупность которых называют нормальными условиями. Если вам не нравятся нормальные условия - живите в ненормальных. Любите жить в тепле - живите на Венере, в холоде - слетайте на Марс.
Что касается металлического водорода, то в этом нет ничего удивитльного. Он ставится химиками в равной степени в первую группу элементов таблицы вместе со щелочными металлами либо в восьмую с благородными газами. Получить металлический водород удалось недавно. Это связано только с техническими проблемами.
Автор: Digger 27.11.2018, 19:35
А в чем вопрос-то? Все чистые металлы действительно имеют кристаллическое строение в твердой фазе, а в жидкой, разумеется, нет. При чем тут шарообразная форма? И еще: не СЧИТАЕТСЯ, что металлы имеют кристаллическое строение, а НАБЛЮДАЕТСЯ невооруженным глазом, в лупу или в микроскоп.
Вопрос в том, что заставляет вещества в жидкой фазе образовывать шарообразную форму.
Не станете же Вы утверждать, что стремление вещества образовывать шарообразную форму - это врождённое свойство.
А коли не станете, то тогда Вам придётся признать наличие сил притяжения между атомами и молекулами в жидкой фазе, а не только в "истинно твёрдой".
И тогда Вам придётся дезавуировать Ваше утверждение:
"В аморфных телах силы притяжения и отталкивания между частицами действуют как и в жидкостях, а в кристаллических телах - как в истинно твердом теле".
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164163
Автор: mechanic 28.11.2018, 4:57
А коли не станете, то тогда Вам придётся признать наличие сил притяжения между атомами и молекулами в жидкой фазе, а не только в "истинно твёрдой".
И тогда Вам придётся дезавуировать Ваше утверждение:
А кто Вам сказал, что это врожденное свойство? Я такого не говорил. Шарообразная форма (в отсутствии прочих сил, нарушающих ее) макроскопически объясняется силами поверхностного натяжения жидкости, причина которых лежит в силах молекулярного взаимодействия, к изучению которых мы еще не приступали.
В завершении макроскопического обзора агрегатных состояний вещества рассмотрим фазовые переходы однокомпонентного вещества.
Переход химически однородного (однокомпонентного) простого тела из одного вида агрегатного состояния в другое характеризуется диаграммой агрегатных состояний — фазовой диаграммой .
[attachment=263:p0044.png]
Переход тела из жидкого состояния (II) в газообразное (пар III) при постоянной температуре протекает с сообщением тепла и называется процессом испарения (кипения); обратный процесс превращения пара (III) в жидкость (II), протекающий с отъемом того же количества тепла, называется конденсацией.
Переход вещества из твердого состояния (I) в жидкое (II) называется плавлением (обратный процесс— затвердевание). Точка пересечения линий испарeния и плавления в координатах давление – температура (точка А на рис. 10) называется тройной точкой ; давление и температура однокомпонентного вещества в тройной точке (P_A,t_A) принадлежит к числу термодинамических констант этого вещества (например, тройная точка воды характеризуется следующими данными: t_A=+0,01℃; P_A=4,58 мм рт.=0,00623 кГ/〖см〗^2).
В тройной точке берет начало линия возгонки или сублимации (переход твердого вещества в газ).
Линии фазовых превращений в координатах давление —температура (рис. 10) являются изображениями термодинамического равновесия двухфазовых систем: линия испарения—равновесие пара и жидкости (насыщенный или влажный пар); линия плавления — равновесие жидкой и твердой фаз; линия сублимации — равновесие пара (газа) и твердой фазы. Уравнение каждой линии фазовых превращений 〖(φ〗_i) характеризует зависимость температуры рассматриваемого фазового превращения от давления (или наоборот).
Теплоты испарения, плавления и сублимации есть теплоты изотермических превращений, т. е. превращений, протекающих без изменения температуры вещества, поэтому обычно они называются скрытыми теплотами фазовых превращений (скрытые теплоты испарения, плавления и сублимации).
Автор: mechanic 28.11.2018, 5:34
Продолжение предыдущего сообщения
Основным термодинамическим (феноменологическим) признаком различия видов агрегатного состояния вещества является наличие энергетической границы между фазами: теплота испарения как граница между жидкостью и ее паром и теплота плавления как граница между твердым веществом и жидкостью.
По мере повышения давления различие удельных объемов и прочих физических характеристик равновесных элементов — кипящей жидкости и сухого насыщенного пара — уменьшается, а вместе с тем уменьшается и величина теплоты испарения. В критической точке K(конечная точка линии испарения) исчезают основные различия между жидкостью и ее паром: удельные объемы и прочие характеристики кипящей жидкости и сухого насыщенного пара равны, а скрытая теплота испарения обращается в нуль (r_k=0).
Параметры критической точки:
P_k — критическое давление, при котором и выше которого жидкость не может быть превращена в пар;
t_k-критическая температура, при которой и выше которой пар не может быть сконденсирован.
На фазовой диаграмме однокомпонентного вещества в соответствии с определениями критических параметров нанесены области жидкости и пара, причем оказывается, что критическая точка является началом условных координат новой области —области закритического состояния (P≥P_k;t≥t_k) в пределах которой вещество может быть только в однофазовом состоянии.
Переход из состояния жидкого (1) в газообразное (2) возможен, помимо прямого пути (1 - 2), также и через закритическую область (1 - 1' - 2' - 2) путем непрерывных изменений, без прохождения энергетического барьера (испарение) и, следовательно, без изменения агрегатного состояния.
Аналогично, переход из жидкого состояния в твердое можно осуществить через переходную однофазовую область пластического состояния.
Таким образом, представляется возможным осуществить переход из любого однофазового исходного состояния (твердого, жидкого, газообразного) в любое однофазовое конечное (твердое, жидкое, газообразное) путем непрерывных изменений, помимо фазовых энергетических барьеров (испарение, плавление), что является условным признаком непрерывности однофазового состояния вещества .. (источник Белоконь, Н.И. Термодинамика).
Иными словами, можно перевести вещество из твердого в газообразное состояние и наоборот двумя путями: через плавление и кипение или непрерывным путем без фазовых переходов. Вот такие пироги. А теперь подумайте, можно ли опросто и однозначно объяснить все эти явления с помощью дипольных магнитных моментов, прелагаемых Зиновием в параллельной теме основной ветки. Я, лично, о-о-чень сомневаюсь.
Автор: Digger 28.11.2018, 6:34
Ну вот же!
С этого и нужно было начинать:
Что создаёт "силы поверхностного натяжения" в жидкости?!
Принцип причинности, однако.
Что за ерундовина такая - силы действующие между молекулами на поверхности?
Откуда молекулы жидкости узнают, что они находятся на поверхности?
На мой взгляд, не существует никаких сил поверхностного натяжения, а есть силы притяжения между молекулами жидкости, которые действуют как в её толще, так и на поверхности.
Вот их то , по недоразумению, и называют "силами поверхностного натяжения.
В толще жидкости силы притяжения действуют на молекулу со всех сторон, уравновешивая друг друга, а на поверхности, только со стороны соседей, лежащих снизу, и рядом на поверхности, что и создаёт иллюзию т.н. "сил поверхностного натяжения".
Автор: ahedron 28.11.2018, 15:27
Поверхностное натяжение - элементарно. Вспомните пузырьки воздуха в подсолнечном масле... Никакого поверхностного натяжения и тем более притяжения между молекулами нет!
Все тела находятся в среде и если атомные/молекулярные связи подвижны, то тело всегда приобретает форму шара. Среда формирует форму.
Глупенькие ёмаё.
Автор: Digger 28.11.2018, 17:34
Все тела находятся в среде и если атомные/молекулярные связи подвижны, то тело всегда приобретает форму шара. Среда формирует форму.
Глупенькие ёмаё.
Вы не тИАретик, вы пустобрёх и воинствующее невежество.
9. Плавучая игла
Можно ли заставить стальную иглу плавать на поверхности воды, как соломинку? Как
будто бы невозможно: кусочек металла, хотя бы и самый маленький, должен непременно
потонуть в воде. Так думают многие, и если вы думаете так же, то следующий опыт заставит
вас переменить свое мнение.
Возьмите обыкновенную, только не слишком толстую швейную иголку, обмажьте ее
слегка маслом или жиром и положите аккуратно на поверхность воды в ведерке или стакане.
К вашему изумлению, игла не пойдет ко дну, а будет держаться на поверхности, наглядно
опровергая всеобщую уверенность в том, что игла не может плавать.
Почему же, однако, она не тонет? Ведь сталь все-таки тяжелее воды? Безусловно, в 7–8
раз тяжелее, и, чтобы плавать, игла должна, по физическому закону плавания, вытеснять
воды во столько же раз больше объемом, чем сама занимает. В нашем случае так и есть: если
вы внимательно рассмотрите поверхность воды возле вашей плавающей иглы, то увидите,
что близ нее вода образует вогнутость, небольшую долину, на дне которой и лежит игла (как
показано в разрезе на рисунке в левом нижнем углу рисунка). Изгибается же водная
поверхность возле нашей иглы потому, что игла, покрытая тонким слоем жира, не
смачивается водой. Вы заметили, вероятно, что когда у вас руки жирные, то вода, налитая на
них, оставляет кожу сухой, т. е. не смачивает ее. Перья гуся и всех вообще плавающих птиц
всегда покрыты жиром, выделяемым особой железой; вот почему вода не пристает к ним
(«что с гуся вода»). Оттого-то без мыла – которое растворяет слой жира и удаляет его с
кожи, – нельзя вымыть жирных рук даже и горячей содой. Жирная иголка тоже не
смачивается водой и потому оказывается на дне водяной лощинки, объем которой настолько
превышает объем иглы, что она поддерживается выталкивающей силой жидкости, как
стальной дредноут на океане.
Так как руки наши всегда немного жирны, то и без намеренного обмазывания жиром
игла в наших руках тоже покрыта тонким слоем его. Поэтому можно заставить иглу плавать,
и не покрывая ее специально жиром, – надо только изловчиться очень осторожно положить
ее на воду. Это можно сделать так: положить иглу на лоскуток папиросной бумаги, а затем,
постепенно отгибая вниз края лоскутка другой иглой, погрузить всю бумажку под воду.
Лоскуток упадет на дно, а игла останется на поверхности.
Если теперь вам случится наблюдать насекомое водомерку, шагающую по воде «яко по
суху» (см. рис. на стр. 32, внизу), то вы уже не будете поставлены в тупик этим фактом, а
догадаетесь, что лапки насекомого покрыты жиром и оттого не смачиваются водой. Шесть
лапок водомерки, вместе взятые, вытесняют, благодаря этому, такой объем воды, который
весит столько, сколько само насекомое, и тогда оно поддерживается на поверхности по мере
движения.
Я.И. Перельман "Для юных физиков. Опыты и развлечения"
Что если не силы притяжения между молекулами жидкости определяют её прочность разрыв?
Что если не они же удерживают стальную иголку на поверхности воды?
Автор: vps137 28.11.2018, 19:52
Что если не силы притяжения между молекулами жидкости определяют её прочность разрыв?
Что если не они же удерживают стальную иголку на поверхности воды?
Перельман дал описание явления. Главным в нём, на мой взгляд, является указание на то, что поверхность воды под иглой является вогнутой. С точки зрения силы поверхностного натяжения это означает, что эта сила направлена к центру кривизны этой вогнутости. Вес иглы уравновешен этой силой.
Капля воды имеет выпуклую поверхность и сила поверхностного натяжения направлена внутрь, тоже в центр кривизны.
Автор: Digger 28.11.2018, 20:31
Капля воды имеет выпуклую поверхность и сила поверхностного натяжения направлена внутрь, тоже в центр кривизны.
Сюр какой-то.
А что создаёт силу поверхностного натяжения?!
Неужто вогнутость?
Вогнутость следствие, а не причина.
Причина всех физических процессов - сила.
Если игла давит на поверхность воды силой веса, то какая сила её уравновешивает, не давая игле утонуть?
Автор: ahedron 28.11.2018, 20:58
Digger, За языком своим следи мудень.
Автор: vps137 29.11.2018, 3:50
Если игла давит на поверхность воды силой веса, то какая сила её уравновешивает, не давая игле утонуть?
Варяг, ваша точка зрения является устаревшей - лет на триста. Сейчас говорят о взаимодействии. Взаимодействии зарядов между собой, о взаимодействии зарядов с полями, о взаимодействии полей. Некоторые сюда приплетают эфир, торсионные поля и божий промысел. Я считаю, что это всё происки 4D материи. Сила - это обобщение. В том числе, и сила поверхностного натяжения. Для объяснения явлений можно выбирать что угодно - лишь бы объясняло. А верное объяснение или нет, покажут наши потомки (если покажут!).
Автор: Digger 29.11.2018, 6:49
Уж да уж!
Так ведь ваши фантазии о 4-D материи - и есть попытка описания Эфира.
Корявая, безграмотная, но Эфира (гипотетической среды, являющейся передатчиком и источником всех силовых "взаимодействий".
"Взаимодействие в физике, воздействие тел или частиц друг на друга, приводящее к изменению состояния их движения. В механике Ньютона взаимное действие тел друг на друга количественно характеризуется силой".
(БСЭ)
По вашему, БСЭ 300 лет?
Как количественно охарактеризовать ваше "взаимодействие", если не силой?!
Автор: vps137 29.11.2018, 8:13
Так ведь ваши фантазии о 4-D материи - и есть попытка описания Эфира.
Корявая, безграмотная, но Эфира (гипотетической среды, являющейся передатчиком и источником всех силовых "взаимодействий".
Опять настаиваите на лживом утверждении. У меня не фантазии, а гипотеза, которая находит подтверждение в самых разных областях физики.
В чём вы, Варяг, усматриваете безграмотность? В том, что не цитирую Ньютона?
(БСЭ)
По вашему, БСЭ 300 лет?
Как количественно охарактеризовать ваше "взаимодействие", если не силой?!
Механика - это не вся физика. В других её разделах нет никаких тел, в гидродинамике, напр.
Взаимодействие характеризуется функцией Лагранжа или функцией Гамильтона. Могут быть и другие варианты. Сила - это обобщение ускорений, которое получает тело от различных источников.
Автор: Digger 29.11.2018, 9:39
В чём вы, Варяг, усматриваете безграмотность? В том, что не цитирую Ньютона?
Механика - это не вся физика. В других её разделах нет никаких тел, в гидродинамике, напр.
Взаимодействие характеризуется функцией Лагранжа или функцией Гамильтона. Могут быть и другие варианты. Сила - это обобщение ускорений, которое получает тело от различных источников.
Механика - фундамент физики!
Выбрасывая из физики понятие "сила", вам не остаётся ничего иного, как отказаться и от понятий "работа" и "энергия".
Физика без сил - бессильная физика.
Ваш отказ от понятия "сила". и её подмена "функцией Лагранжа или функцией Гамильтона", и есть демонстрация вашей физической безграмотности, которую вы прячете под наукообразной болтовнёй.
Причина всех! физических процессов - "сила".
Функции Лагранжа или Гамильтона не являются причиной физических процессов, а их математическим описанием.
Таким образом, совершенно очевидно, что вы не понимаете разницу между причиной и следствием.
Поэтому все ваши "гипотезы", не более чем безграмотные фантазии.
Автор: vps137 29.11.2018, 10:23
Выбрасывая из физики понятие "сила", вам не остаётся ничего иного, как отказаться и от понятий "работа" и "энергия".
Физика без сил - бессильная физика.
Ваш отказ от понятия "сила". и её подмена "функцией Лагранжа или функцией Гамильтона", и есть демонстрация вашей физической безграмотности, которую вы прячете под наукообразной болтовнёй.
Причина всех! физических процессов - "сила".
Функции Лагранжа или Гамильтона не являются причиной физических процессов, а их математическим описанием.
Таким образом, совершенно очевидно, что вы не понимаете разницу между причиной и следствием.
Поэтому все ваши "гипотезы", не более чем безграмотные фантазии.
Во-первых, Варяг, никто понятие сила никуда не выбрасывает.
Во-вторых, сила - это тоже математическое описание процессов, механических процессов.
В-третьих, поэтому фантазёром являетесь вы, раз путаетесь в азбучных истинах.
Автор: Digger 29.11.2018, 11:33
Во-вторых, сила - это тоже математическое описание процессов, механических процессов.
В-третьих, поэтому фантазёром являетесь вы, раз путаетесь в азбучных истинах.
Вы писали:
"Варяг, ваша точка зрения является устаревшей - лет на триста. Сейчас говорят о взаимодействии. Взаимодействии зарядов между собой, о взаимодействии зарядов с полями, о взаимодействии полей. Некоторые сюда приплетают эфир, торсионные поля и божий промысел. Я считаю, что это всё происки 4D материи. Сила - это обобщение. В том числе, и сила поверхностного натяжения. Для объяснения явлений можно выбирать что угодно - лишь бы объясняло. А верное объяснение или нет, покажут наши потомки (если покажут!)".
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164210
Как говорится, "ни убавить, ни прибавить"
Сила не "обобщениие" - сила, по определению, мера механического взаимодействия двух тел.
Т.е. вы не знаете основополагающего определения физики, но при этом обвиняете меня в непонимании азбучных истин.
Вы даже не знаете основной цели науки "физика", коли пишете, что "Для объяснения явлений можно выбирать что угодно - лишь бы объясняло".
Цель науки не "объяснение" (объяснить можно и при помощи божьего промысла, который тоже
объяснение), а создание теорий не противоречащих экспериментальным фактам, и обладающих предсказательной силой.
Какая предсказательная сила у вашей модели 4-D материи?
А коли ваша теория не обладает такой силой, то она является фантазией.
КОНЕЦ СВЯЗИ.
Автор: vps137 29.11.2018, 12:42
"Варяг, ваша точка зрения является устаревшей - лет на триста. Сейчас говорят о взаимодействии. Взаимодействии зарядов между собой, о взаимодействии зарядов с полями, о взаимодействии полей. Некоторые сюда приплетают эфир, торсионные поля и божий промысел. Я считаю, что это всё происки 4D материи. Сила - это обобщение. В том числе, и сила поверхностного натяжения. Для объяснения явлений можно выбирать что угодно - лишь бы объясняло. А верное объяснение или нет, покажут наши потомки (если покажут!)".
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164210
Как говорится, "ни убавить, ни прибавить"
Сила не "обобщениие" - сила, по определению, мера механического взаимодействия двух тел.
Т.е. вы не знаете основополагающего определения физики, но при этом обвиняете меня в непонимании азбучных истин.
Вы даже не знаете основной цели науки "физика", коли пишете, что "Для объяснения явлений можно выбирать что угодно - лишь бы объясняло".
Цель науки не "объяснение" (объяснить можно и при помощи божьего промысла, который тоже
объяснение), а создание теорий не противоречащих экспериментальным фактам, и обладающих предсказательной силой.
Какая предсказательная сила у вашей модели 4-D материи?
А коли ваша теория не обладает такой силой, то она является фантазией.
КОНЕЦ СВЯЗИ.
Варяг, вы опять всё привираете. Откуда у человека такая злоба? Вы - украинец?
Я ничего не говорил про цель науки. Что такое сила я знаю не хуже вас.
Предсказания, которые следуют из модели 4D , очевидны. Поэтому я не собираюсь их озвучивать.
Адью.
Автор: RudnikV 30.11.2018, 6:50
Наверное одним из наглядных примеров применения поверхностного натяжения является процесс получения свинцовой дроби. На какой-то высоте находится емкость с расплавленным свинцом, откуда как-то умудряются выжимать свинец по каплям А снизу направляют встречный поток холодного воздуха. Пока свинцовая капля летит вниз, она принимает форму шара. Вроде бы так.
Автор: Digger 30.11.2018, 8:36
Свинцовая капля принимает форму шара не пока летит вниз, а почти сразу, а летит она вниз 30-40 метров, чтобы успеть остыть и не расплющиться при ударе о поверхность воды.
В том, что именно силы поверхностного натяжения заставляют каплю свинца принимать шарообразную форму, сомневаться не приходится.
Вопрос-то в другом: что создаёт эти силы, и какова их природа?
Автор: mechanic 2.12.2018, 5:11
Вопрос-то в другом: что создаёт эти силы, и какова их природа?
Это уже прогресс. Силы поверхностного натяжения получили право на существование. В отсутсвие посторонних сил, в частности тяготения, жидкость принимает шарообразную форму, будь- то капля расплавленного свинца, падающая с башни, капля дождя или жидкость пролитая в космическом корабле. Все эти жидкости удерживаются в шарообразном состоянии силами поверхностного натяжения. Это опытный факт. При наличии сил тяготения, растущих в кубической зависимости от размера капли, тогда как силы поверхностного натяжения растут в квадратичной зависимости шарик сплющивается и в конце концов растекается, образуя горизонтальную поверхность.
Попробую объяснить возникновение сил, аналогичных силам поверхностного натяжения "на пальцах", используя следующую модель.
Представьте себе, что вы надуваете воздушный шарик. При этом резиновая пленка начинает растягиваться и тем сильнее, чем больше становится диаметр шара. В поперечном разрезе эта пленка представляет собой окружность. Выделим на этой окружности три соседние точки на небольшом расстоянии друг от друга ( рисунка не будет: мой сканер вышел из строя, так что рисуйте сами или представляйте мысленно) и соедините выделенные точки отрезками: первую со второй, вторую - с третьей. Вдоль этих линий нарисуйте векторы растягивающих сил в направлениях от второй точки к первой и к третьей. Равнодействующая этих двух сил будет направлена к центру шара. Можно посмотреть на эту картину и с другой стороны. Сила, направленная к центру, раскладывается на две силы растягивающие пленку. Представьте теперь , что шар расширяется, угол между силами растяжения увеличивается и стремится к 180 градусам. При этом кривизна поверхности приближается к плоскости. В пределе силы растяжения. действующие на среднюю точку будут уравновешивать друг друга.
Теперь перейдем к жидкости. В отличие от газов расстояние между молекулами жидкостей на порядок меньше, и между ними наблюдаются силы взаимного притяжения, о природе которых мы пока не говорим. Эти силы также называются Ван-дер-Ваальсовскими силами.
Жидкость характеризуется наличием поверхности. при прохождении которой скачкообразно меняется ее плотность. Это сильно влияет на ее свойства. Молекулы жидкости, расположенные в поверхностном слое, находятся в состоянии отличном от молекул, расположенных в его толще. (см. рисунок). Молекулярные силы взаимодействия действуют на очень коротких расстояниях, определяемых сферой молекулярного действия (порядка 10^-9). Молекулы расположенные в толще жидкости окружены со всех сторон аналогичными молекулами и их силы взаимодействия взаимно компенсируются. В ином положении находятся молекулы поверхностного слоя. Они будут взаимодействовать в пределах сфер молекулярного взаимодействия с большим количеством молекул, расположенных со стороны жидкости, с одной стороны, и небольшим количеством молекул вещества в паровой фазе, с другой. Лежащие в поверхностном слое молекулы притягиваются не только молекулами , расположенными ниже их, но и своими соседями. В результате этого в поверхностном слое возникает сила, величина которой зависит от интенсивности взаимодействия молекул данной жидкости. Для количественной оценки этой силы ее относят к единице длины линии, расположенной на поверхности. Эта величина, измеряемая в Н/м, носит название - коэффициент поверхностного натяжения.
[attachment=266:p0099__2_.jpg]
Автор: Digger 2.12.2018, 9:05
Попробую объяснить возникновение сил, аналогичных силам поверхностного натяжения "на пальцах", используя следующую модель.
Представьте себе, что вы надуваете воздушный шарик. При этом резиновая пленка начинает растягиваться и тем сильнее, чем больше становится диаметр шара. В поперечном разрезе эта пленка представляет собой окружность. Выделим на этой окружности три соседние точки на небольшом расстоянии друг от друга ( рисунка не будет: мой сканер вышел из строя, так что рисуйте сами или представляйте мысленно) и соедините выделенные точки отрезками: первую со второй, вторую - с третьей. Вдоль этих линий нарисуйте векторы растягивающих сил в направлениях от второй точки к первой и к третьей. Равнодействующая этих двух сил будет направлена к центру шара. Можно посмотреть на эту картину и с другой стороны. Сила, направленная к центру, раскладывается на две силы растягивающие пленку. Представьте теперь , что шар расширяется, угол между силами растяжения увеличивается и стремится к 180 градусам. При этом кривизна поверхности приближается к плоскости. В пределе силы растяжения. действующие на среднюю точку будут уравновешивать друг друга.
Теперь перейдем к жидкости. В отличие от газов расстояние между молекулами жидкостей на порядок меньше, и между ними наблюдаются силы взаимного притяжения, о природе которых мы пока не говорим. Эти силы также называются Ван-дер-Ваальсовскими силами.
Жидкость характеризуется наличием поверхности. при прохождении которой скачкообразно меняется ее плотность. Это сильно влияет на ее свойства. Молекулы жидкости, расположенные в поверхностном слое, находятся в состоянии отличном от молекул, расположенных в его толще. (см. рисунок). Молекулярные силы взаимодействия действуют на очень коротких расстояниях, определяемых сферой молекулярного действия (порядка 10^-9). Молекулы расположенные в толще жидкости окружены со всех сторон аналогичными молекулами и их силы взаимодействия взаимно компенсируются. В ином положении находятся молекулы поверхностного слоя. Они будут взаимодействовать в пределах сфер молекулярного взаимодействия с большим количеством молекул, расположенных со стороны жидкости, с одной стороны, и небольшим количеством молекул вещества в паровой фазе, с другой. Лежащие в поверхностном слое молекулы притягиваются не только молекулами , расположенными ниже их, но и своими соседями. В результате этого в поверхностном слое возникает сила, величина которой зависит от интенсивности взаимодействия молекул данной жидкости. Для количественной оценки этой силы ее относят к единице длины линии, расположенной на поверхности. Эта величина, измеряемая в Н/м, носит название - коэффициент поверхностного натяжения.
[attachment=266:p0099__2_.jpg]
Чтобы прогресс, действительно, наступил, следует честно и открыто признать, что никаких самостоятельных сил поверхностного натяжения не существует, е есть силы притяжения между молекулами жидкости, которые-то и создают эффект поверхностного натяжения:
http://physicsbooks.narod.ru/c-news/Aleshkevich_pp184-186.pdf
Поверхностное натяжение. Постоянство объема жидкости обеспечивается значительными силами межмолекулярного притяжения. Этот объем имеет ограничивающую его поверхность. Равнодействующая сил, приложенных к отдельной молекуле, будет равна нулю, если молекула находится в глубине объема. На молекулу, находящуюся вблизи поверхности, будет действовать равнодействующая сила, перпендикулярная поверхности и направленная внутрь жидкости"
(Алешкевич В.А. Курс общей физики. Молекулярная физика.—М.: ФИЗМАТЛИТ, 2016. — 312 с. — ISBN 978-5-9221-1696-1)
А сделав этот шаг, мы сможем сделать и другой - попытаться понять природу этих сил.
http://physicsbooks.narod.ru/c-news/Aleshkevich_pp16-17.pdf
"На больших расстояниях между атомами силы их взаимодействия пренебрежимо малы. При сближении атомы начинают действовать друг на друга,
при этом, как отмечалось ранее, возникают силы двух типов: притяжения и отталкивания".
(Там же)
В учебниках пишут, что силы притяжения, и силы отталкивания между молекулами - это т.н. "силы Ван дер Ваальса", и которые имеют электромагнитную природу.
Но, во первых, силы одной природы не монут быть одновременно силами притяжения и силами отталкивания, а, во-вторых, не могут иметь разную зависимость от расстояния между атомами и молекулами.
Т.е., вопрос о природе сил притяжения между атомаи и молекулами пока остаётся без ответа.
Автор: ahedron 2.12.2018, 14:21
Осталось только понять, как НЕЙТРАЛЬНЫЕ молекулы притягиваются друг к другу... А никак!
Электрических и магнитных сил нету, остаются механические - неужели ручками? Хммм... у них жИ нет ручек, а как тогда?
Госпиди, какие же вы гении (нет).
Автор: Тихомиров Евгений 2.12.2018, 19:23
Про силы поверхностного натяжения надо спрашивать у посла высокоразвитй цивилизации Ивана Васильевича Пономаренко. Только он может видеть все на атомно-молекулярном уровне. Называть же эти силы Ван дер Ваальса, понимания о их природе не даёт. Но по-видимому эти силы всё-таки электромаагнитного характера, но проявляются на атомном и молекулярном уровне.
Автор: Patent 3.12.2018, 6:17
Может, стоит ответами на следующие вопросы расшевелить своё воображение и подойти к проблеме с другой стороны.
Выберите нужный ответ из трёх вариантов.
1. С мениском воды на стенке стеклянного стакана все знакомы.
Смачивание, происходит ?:
1. При наличии сил притяжения молекул воды к стеклу.
2. При наличии сил отталкивания молекул воды от стекла.
3. При отсутствии каких-либо сил между молекулами воды и стекла.
2. Мы знакомы со способностью газов (воздуха и т д.) растворяться в жидкости и в частности в воде.
Растворение воздуха в воде происходит?:
1. При наличии сил притяжения молекул воздуха к молекулам воды.
2. При наличии сил отталкивания между молекулами воздуха и молекулами воды.
3. При отсутствии каких-либо сил между молекулами воздуха и воды.
Автор: Digger 3.12.2018, 7:31
Выберите нужный ответ из трёх вариантов.
1. С мениском воды на стенке стеклянного стакана все знакомы.
Смачивание, происходит ?:
1. При наличии сил притяжения молекул воды к стеклу.
2. При наличии сил отталкивания молекул воды от стекла.
3. При отсутствии каких-либо сил между молекулами воды и стекла.
2. Мы знакомы со способностью газов (воздуха и т д.) растворяться в жидкости и в частности в воде.
Растворение воздуха в воде происходит?:
1. При наличии сил притяжения молекул воздуха к молекулам воды.
2. При наличии сил отталкивания между молекулами воздуха и молекулами воды.
3. При отсутствии каких-либо сил между молекулами воздуха и воды.
Про гидрофобность и гидрофильность, наверное, знаете.
Вот и ответьте, воображательный Вы наш, почему в стеклянной трубке вода образует мениск, а в полиэтиленовой - линзу?
Почему к стеклу молекулы воды притчягиваются, а от полиэтилена отталкиваются?
Автор: Patent 3.12.2018, 8:47
Вот и ответьте, воображательный Вы наш, почему в стеклянной трубке вода образует мениск, а в полиэтиленовой - линзу?
Почему к стеклу молекулы воды притчягиваются, а от полиэтилена отталкиваются?
У меня на эти вопросы ответы есть.
А Вы уклонились от конкретного ответа.
Так какие ответы выбираете?
Без чёткого ответа на эти вопросы продолжение не планируется.
Автор: alal 3.12.2018, 8:59
О, мудрейший из мудрейших! О, просветленнейший из просветленнейших! О, умнейший из умнейших!
Иван Васильевич, снизойди до нас темных и слепых, объясни про силы поверхностного натяжения, освободи от оков коварного Ван дер Ваальса!
Бум благодарны повек, бум!
Автор: Digger 3.12.2018, 11:00
А Вы уклонились от конкретного ответа.
Так какие ответы выбираете?
Без чёткого ответа на эти вопросы продолжение не планируется.
Вопросы мы все задавать мастера.
Мой вопрос о природе сил притяжения между молекулами жидкости вы проигорировали, а вместо ответа задали целую кучу своих вопросов, имеющих косвенное отношение к силам притяжения между молекулами жидкости.
Ккую цель вы ставите перед собой, уводя дискуссию в сторону от обозначенного ранее вопроса?
Автор: Patent 3.12.2018, 11:07
Мой вопрос о природе сил притяжения между молекулами жидкости вы проигорировали, а вместо ответа задали целую кучу своих вопросов, имеющих косвенное отношение к силам притяжения между молекулами жидкости.
Ккую цель вы ставите перед собой, уводя дискуссию в сторону от обозначенного ранее вопроса?
Это вы нежеланием чётко выбрать соответствующий ответ начинаете тему забалтывать.
К чему вопросы - всё выясниться после появления ответов.
Всего-то требуется дать два цифровых ответа.
Автор: Digger 3.12.2018, 11:48
К чему вопросы - всё выясниться после появления ответов.
Всего-то требуется дать два цифровых ответа.
Покуда не дадите ответа на мой вопрос, все ваши вопросы буду игнорировать.
Автор: Patent 3.12.2018, 13:38
Я ясно объяснил, что мои ответы зависят от ваших.
А игнорировать, при этих условиях,самое глупое действие.
Но, это Ваше.
Заставить не могу.
Автор: Digger 3.12.2018, 14:29
А игнорировать, при этих условиях,самое глупое действие.
Но, это Ваше.
Заставить не могу.
Отвечать вопросом на вопрос, вообще-то, не принято.
Хотя, у вас может и по-другому:
Рабинович, а правда, что евреи отвечают вопросом на вопрос? - Кто вам это сказал?
Автор: Patent 3.12.2018, 14:36
Хотя, у вас может и по-другому:
Рабинович, а правда, что евреи отвечают вопросом на вопрос? - Кто вам это сказал?
Много буков.
Я первый задал вопрос.
Автор: alal 3.12.2018, 15:04
Мальчиши-Кибальчиши !
Что же это такая за непонятная страна, в которой даже такие малыши знают Военную Тайну и так крепко держат свое твердое слово ![]()
Автор: Digger 3.12.2018, 15:05
Я первый задал вопрос.
Да вы, любезный, лжец.
Вопрос был задан мной, а вы вместо ответа н него задали кучу своих вопросов.
Идите-ка вы лесом...
Автор: Patent 3.12.2018, 16:03
Вопрос был задан мной, а вы вместо ответа н него задали кучу своих вопросов.
Идите-ка вы лесом...
Я задал сегодня здесь -
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164363
Иди.
Автор: ahedron 3.12.2018, 17:57
Ответ начинается с вопроса... А можно сразу ответ? Или так у вас не принято?
Молекулы не притягиваются и не отталкиваются, за них это делают другие...
Автор: Patent 3.12.2018, 18:12
Молекулы не притягиваются и не отталкиваются, за них это делают другие...
У меня конкретные вопросы. Хотите их изменить, меняйте и задавайте, но уже под своё видение проблемы.
Автор: ahedron 3.12.2018, 19:44
Patent, Мне ни один ответ не подходит. Что мне делать в таком случае?
Как бы можно было воспользоваться третьим вариантом, но там слово между, а это относится к 1-му и 2-му варианту... Потому что МЕЖДУ молекулами никаких сил нет.
Автор: mechanic 3.12.2018, 23:20
Электрических и магнитных сил нету, остаются механические - неужели ручками? Хммм... у них жИ нет ручек, а как тогда?
Госпиди, какие же вы гении (нет).
Вот на этом и остановились в теме, открытой Зиновием. То, что молекулы нейтральны, это примерно то же, что средняя температура по больнице - 36, 6.
Кто их присутствующих в этой теме знает, чем отличаются по своему строению молекулы самых простых веществ, например, Н₂, О₂, Н₂О, и NaCl ? Никто даже не заинтересовался этим вопросом. А без этого элементарного знания и продвигаться дальше некуда.
Автор: ahedron 3.12.2018, 23:53
mechanic, Верный "подкоп", но почему-то я уверен, что ваш ответ мне не подойдёт.
Автор: mechanic 4.12.2018, 6:02
Ответ - не обувь и не фасон, что может подойти или не подойти, а факты и научное знание на данный момент. Другое дело он может не совпасть с чьими-то представлениями на этот счет. А в таких случаях личные амбиции могут затмить разумные доводы и результаты экспериментов. Вопрос не такой простой, чтобы дать однозначный ответ, как это пытаются делать Зиновий и Patent, исходя из своих личных воззрений и гипотез. Дело в том, что молекулы и атомы различных веществ устроены по- разному и нельзя грести все под одну гребенку.
Для того, чтобы хоть немного разобраться в этом вопросе, требуется кое-что усвоить из области химии, точнее из области строения молекул и связях между их атомами, а для детального рассмотрения более сложных случаев необходимы глубокие познания в квантовой механике и смежных науках. Я могу привести только самые простые и наглядные примеры, так как не являюсь специалистом в данной области.
Автор: Digger 4.12.2018, 7:22
Для того, чтобы хоть немного разобраться в этом вопросе, требуется кое-что усвоить из области химии, точнее из области строения молекул и связях между их атомами, а для детального рассмотрения более сложных случаев необходимы глубокие познания в квантовой механике и смежных науках. Я могу привести только самые простые и наглядные примеры, так как не являюсь специалистом в данной области.
Для усвоения (потребления), нужно знать, что потребляемое не навредит твоему здоровью.
Откуда у Вас такая уверенность, что химия даёт нам правильные представления о строении молекул?
Простой пример:
Расстояния между атомами алюминия (металл) ок. 2 ангстрем.
Удивительно, но факт, что для корунда (Al2O3) расстояния между молекулами те же 2 ангстрема.
Но молекула корунда состоит из 5 атомов.
Вопрос: как нужно уложить 10 атомов, чтобы они занимали такой же объём, как и два атома?
Напомню, что в современной химии считается, что атомы составляющие молекулу, прилеплены один к другому при помощи связей, образованных т.н. "валентными электронами". А размеры самих атомов ок. 1 ангстрема.
(ангстрем 10-10 м)
P.S.
Рассчитать межатомные и межмолекулярные расстояния сможет даже школьник:
Для этого нужно знать атомный (молекулярный) вес вещества, его плотность, и помнить, что в 1 моле любого в-ва содержится 6,022*1023 атомов или молекул.
(моль - количество вещества в граммах численно равное его атомному (молекулярному весу).
Например, 1 моль алюминия весит 27 грамм, а корунда 2*27+3*16 = 102 грамма.
Автор: Patent 4.12.2018, 7:32
Как бы можно было воспользоваться третьим вариантом, но там слово между, а это относится к 1-му и 2-му варианту... Потому что МЕЖДУ молекулами никаких сил нет.
Успокойтесь. Если ни один из моих вопросов вам не подходит, значит они не для Вас.
Они только для тех, кто может выбрать первый ответ.
Автор: ahedron 4.12.2018, 15:00
Patent, Жесть... а как же истина, вас она не интересует?
Кто определил расстояния между молекулами и атомами, если их даже никто не видел? То что мы можем видеть, это оболочки атомов и молекул и они, естественно у всего примерно одинаковые... на глаз не определить, даже на "глаз" электронного микроскопа.
Автор: mechanic 5.12.2018, 18:07
Простой пример:
Расстояния между атомами алюминия (металл) ок. 2 ангстрем.
Удивительно, но факт, что для корунда (Al2O3) расстояния между молекулами те же 2 ангстрема.
Но молекула корунда состоит из 5 атомов.
Вопрос: как нужно уложить 10 атомов, чтобы они занимали такой же объём, как и два атома?
Напомню, что в современной химии считается, что атомы составляющие молекулу, прилеплены один к другому при помощи связей, образованных т.н. "валентными электронами". А размеры самих атомов ок. 1 ангстрема.
(ангстрем 10-10 м)
У меня есть подозрение, что у вас неправильное представление о том , что в химии написано, а отсюда и полный вздор, который вы написали. Допустим , условно, что два атома алюминия это два теннисных мячика и расстояние между ними 2см, а две молекулы корунда это два волейбольных мяча, расстояние между которыми тоже 2см. И с каких дел у вас два атома занимают тотже объем, что и две молекулы. Дайте ссылочку, если я неправ.
И заодно прочитайте http://kilomol.ru/molecula.html
Автор: Digger 5.12.2018, 21:23
И заодно прочитайте http://kilomol.ru/molecula.html
Сдаётся мне, что это вы начитались всякого вздора.
Когда я писал, что расстояние между двумя атомами алюминия 2 ангстрема, то имел ввиду, что это расстояие между центрами этих атомов.
Если размер атома алюминия около 1 анстрема, то получается, что между ними пустой промежуток тоже порядка 1 ангстрема.
Но и для молекул корунда расстояние между их центрами те же 2 ангстрема, поэтому я и спрашиваю вас: как нужно уложить 10 атомов, чтобы они заняли такой объём, как и два атома?
Я вам пишу то, что получается из расчётных данных, а вы мне суете учебник, как-будто в учебниках прописана истина в последней инстанции.
Автор: mechanic 6.12.2018, 5:33
Так вот и дайте расчет, только обоснуйте все исходные данные и понятия со ссылками на источники. В частности, надо обосновать, что принято считать расстоянием между атомами и молекулами, а не заниматься самодеятельностью.
Автор: Digger 6.12.2018, 10:12
Извольте:
http://physicsbooks.narod.ru/c-news/AluminiumCorundum.xls
Из этого расчёта получается, что расстояния между центрами атомов алюминия в 1,36 раза меньше чем расстояния между центрами молекул корунда, состоящих не из одного, а из пяти атомов.
Соответственно объём, занимаемый одним атомом алюминия всего в 2,5 раза меньше, чем объём занимаемый 5 атомами молекулы корунда.
Если сложить теннисные мячи максимально плотно, то объём занимаемый сотней таких мячей будет в пять раз меньше, чем занимаемый пятьюстами.
В пять, а не в 2,5!
Где деньги, Зин?
Автор: ahedron 6.12.2018, 15:17
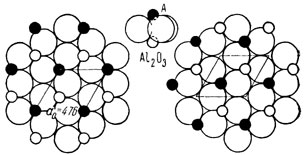
Автор: Digger 6.12.2018, 16:10

Кроме как по комиксам, поколение ЕГЭ изучать физику принципиально не может.
Размеры атомов кислорода ничуть не меньше, чем размеры атомов алюминия.
Док-во плотность кислорода в жидкой и твёрдой фазах.
В жидкой 1,41 г/см3, в твёрдой 1,27 г/см3.
Т.е. один моль (6,022*1023 атомов кислорода) в твёрдой фазе занимают такой же объём, как и один моль алюминия.
А в комиксе атомы кислорода нарисованы в разы меньшими атомов алюминия.
Автор: Digger 6.12.2018, 20:44
Четыре с лишком часа уже прошло, а "германа" всё нет.
В своём ответе я лажанулся, написав, что 6,022*1023 атомов кислорода занимают такой же объём в твёрдой фазе, как и столько же атомов алюминия. Правильно было написать, что 6,022*1023 молекул , а не атомов кислорода занимают такой же объём как один моль алюминия.
Хотел было сразу исправить, но потом подумал, а как "поколение ЕГЭ и пепси" среагирует на мою лажу?
Получается, что проглотило не поперхнувшись, как до этого глотало комиксы.
Вот такие знания у этого хамоватого и охочего до картинок поколения. ![]()
Автор: mechanic 6.12.2018, 21:52
А разница во времени с Москвой у меня 8 часов и можно еще подумать, что у меня с утра больше других дел нет как сидеть на форуме.
Теперь по поводу ссылки. Совершенно непонятен источник. да и расчета нет никакого. Каждая цифра должна быть обоснована источником, откуда она взята. Нет и самого расчета а приведены только его результаты. И еще : термин расстояние между атомами или молекулами должен иметь дефиницию. Если это межъядерное расстояние, то так лучше его и называть, а если это расстояние между молекулами или атомами - это зазор или перекрытие (взаимопроникновение) или зазор со знаком минус.
Автор: ahedron 7.12.2018, 2:22
Тут столько лажи, что и разбираться в этом говне не хочется.
Почитали бы сначала хоть что такое число Авогадро, а потом подумали, а потом написали.
Сначала написал лажу, потом попытался исправить и снова лажанулся.
Варяг, бросайте эту физику, ну не ваше это... совсем не ваше. ![]()
Автор: Digger 7.12.2018, 7:11
Теперь по поводу ссылки. Совершенно непонятен источник. да и расчета нет никакого. Каждая цифра должна быть обоснована источником, откуда она взята. Нет и самого расчета а приведены только его результаты. И еще : термин расстояние между атомами или молекулами должен иметь дефиницию. Если это межъядерное расстояние, то так лучше его и называть, а если это расстояние между молекулами или атомами - это зазор или перекрытие (взаимопроникновение) или зазор со знаком минус.
Похоже, Вы не в курсе, как делаются вычисления в Excel, и где находятся расчётные формулы. А что касается исходных данных, то они взяты из открытых источников, которые доступны всем, например, из не любимой мной википедии.
Касаемо расстояний межу атомами, то конечно, можно взять и межъядерное, но что тогда считать межъядерным для молекул?
Поэтому, правильнее, на мой взгляд, брать не расстояние, а объём занимаемый атомом или молекулой.
Разделив объём моля вещества на число Авогадро, получим объём занимаемый атомом или молекулой с учётом зазоров между ними.
P.S.
Моё "А "германа" всё нет" адресовалась, отнюдь, не Вам, а представителю поколения ЕГЭ и пепси, к которому Вас нельзя причислить, поскольку в школу Вы пошли сразу после войны.
Автор: ahedron 7.12.2018, 13:50
Неужели я услышал слово моль. Но слово объём снова меня смущает. Разве у молей известны объёмы... А не считается ли число Авогадро через известный объём вещества?
Digger, Не стройте из себя психолога, тут вы тоже ноль!
Разве вы на столько старый, что не попадаете под поколение пепси?
Автор: Digger 7.12.2018, 17:46
Digger, Не стройте из себя психолога, тут вы тоже ноль!
Разве вы на столько старый, что не попадаете под поколение пепси?
Поскольку поколение ЕГЭ в вашем лице, не знает что такое моль, то дабы другие не были введены в заблуждение вашими безграмотными экзерсисами, считаю своим долгом объяснить вам и вам подобным, что моль, по определению - количество вещества в граммах, численно равном его атомному или молекулярному весу.
Объём одного моля рассчитывается исходя из его веса и плотности вещества.
Т.е. объём 1 моля любого вещества есть вес этого моля делённый на плотность этого вещества.
Число Авогадро легко рассчитать зная атомную (молекулярную) массу вещества и массу нуклонов составляющих атом или молекулу этого вещества.
Не существует никакого иного способа точно вычислить число Авогадро.
Т.е. ваше утверждение "А не считается ли число Авогадро через известный объём вещества?" - свидельство вашей вопиющей безграмотности и неимоверного самомнения и наглости.
Видимо, одно является следствием другого.
Через объём вещества (газа) число Авогадро пытались вычислить ещё в середине 19-го века, но точность этих вычислений была крайне невысокой.
И только в 20-м веке, когда научились измерять массу ядер и нуклонов, учёные смогли вычислить современное значение числа Авогадро.
Автор: ahedron 7.12.2018, 19:29
Вы хотите сказать этой темой, что молекула корунда это куб? как и все молекулы вообще, даже ДНК у вас куб... хм... интересное заявление.
Автор: Digger 7.12.2018, 20:09
Поясните ход ваших мыслей шальных: с какого перепугу вы приписываете мне утверждение, что все молекулы, вообще - куб?
Автор: ahedron 7.12.2018, 21:00
Автор: Digger 7.12.2018, 21:21
А вы, видимо считаете, что 500 мячей займут объём не в 5 раз бОльший, нежели сто точно таких же мячей?
Ну и во сколько же раз, по вашему?
Автор: mechanic 8.12.2018, 7:27
Если речь идет о молекулах, то размеры их зависят не только от химического состава, но и от строения и характера связей между атомами. Молекулы могут состоять из атомов одного элемента, например, газы Н₂, О₂, в которых электронные облака сближаются и взаимно пересекаются. Эта связь называется ковалентной. Читайте последний абзац на стр. 114 и см. рис. 26, 27 приложения. (Глинка, Общая химия)
[attachment=268:p0137.png]
Связь может быть ионной, когда молекула состоит из атомов различных элементов, причем один из атомов - щелочной металл, например, Na легко отдает свой электрон из наружного слоя, превращаясь в положительно заряженный ион Na+, а другой элемент - сильный электроотрицательный металлоид - Cl, принимает его в свои объятья и образует отрицательно заряженный ион Cl- . Оба иона, имеющие противоположные заряды, притягиваются друг к другу, образуя молекулу NaCl. Соединившись в молекулу, два разноименно заряженных иона сохраняют свою способность взаимодействовать с другими молекулами, так как представляют собой систему из двух одинаковых по величине, но противоположных по знаку зарядов, создающих электрическое поле. Вот вам и "нейтральные молекулы" ( в среднем по колхозу). Возвращаясь к ковалентной связи (рис. 27) следует отметить , что химическая связь двух атомов водорода является результатом взаимопроникновения (перекрывания) электронных облаков, происходящего при сближении атомов. Вследствие такого перекрывания плотность отрицательного заряда в межъядерном пространстве возрастает, а положительно заряженные ядра притягиваются к области перекрывания электронных облаков. Это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов и таким образом образуется молекула. Как видите, приведенные два способа образования молекул принципиально различны. Но это не все. Есть и другие типы связей. Расмотрим их в следующий раз. А пока что отметим, что атом практически пуст и его электронное облако может деформироваться при образовании молекул.
Автор: Digger 8.12.2018, 8:53
[attachment=268:p0137.png]
Связь может быть ионной, когда молекула состоит из атомов различных элементов, причем один из атомов - щелочной металл, например, Na легко отдает свой электрон из наружного слоя, превращаясь в положительно заряженный ион Na+, а другой элемент - сильный электроотрицательный металлоид - Cl, принимает его в свои объятья и образует отрицательно заряженный ион Cl- . Оба иона, имеющие противоположные заряды, притягиваются друг к другу, образуя молекулу NaCl. Соединившись в молекулу, два разноименно заряженных иона сохраняют свою способность взаимодействовать с другими молекулами, так как представляют собой систему из двух одинаковых по величине, но противоположных по знаку зарядов, создающих электрическое поле. Вот вам и "нейтральные молекулы" ( в среднем по колхозу). Возвращаясь к ковалентной связи (рис. 27) следует отметить , что химическая связь двух атомов водорода является результатом взаимопроникновения (перекрывания) электронных облаков, происходящего при сближении атомов. Вследствие такого перекрывания плотность отрицательного заряда в межъядерном пространстве возрастает, а положительно заряженные ядра притягиваются к области перекрывания электронных облаков. Это притяжение преобладает над взаимным отталкиванием одноименно заряженных электронов и таким образом образуется молекула. Как видите, приведенные два способа образования молекул принципиально различны. Но это не все. Есть и другие типы связей. Расмотрим их в следующий раз. А пока что отметим, что атом практически пуст и его электронное облако может деформироваться при образовании молекул.
Двигаться нужно от простого к сложному, а Вы нагородили здесь ионные, коваоентные связи, заряды.
Вы сами-то никогда не задумывались над абсурдностью современных представлений о химической связи, образованной т.н. "валентными электронами".
Считается, что электроны - отрицательно заряжены, а из этого следует, что они не млгут спариваться, но только отталкиваться. Не химия, а какой-то гей-парад а Вашингтоне.
Давайте попробуем абстрагироваться от химических связей, и посмотреть на строение в-ва с другой стороны:
Вам наверняка известно, что углерод может существовать в трёх различных аллотропных модификациях: сажа, графит и алмаз.
За каким лешим электронам двух атомов углерода нужно спариваться, если атомы углерода и так электронейтральны?
Давайте попробуем посмотреть на строение молекул с другой стороны:
Поскольку Вы знаете и понимаете термодинамику, то Вас наверняка должен заинтересовать вопрос о том, почему теплоёмкость выше перечисленных аллотропных модификаций существенно различается.
Так, например, мольная теплоёмкость алмаза составляет примерно 6 Дж/моль*К, графита 8, а сажи 25 Дж/моль*К !
Любопытная получается картина: в алмазе самые прочные связи, т.е. на раскачку атома углерода в алмазе нужно затратить больше энергии, нежели в графите, и уж тем болеее в саже.
Но видим-то мы совсем иное!
Как,по-Вашему, можно объяснить сей неоспоримый факт?
Или другой пример:
Теплоёмкость воды в твёрдом (лёд) и газообразном (пар) агрегатном состоянии одинакова, а вот в жидкой фазе её теплоёмкость выше в 2,5 раза.
Вопрос: какая-такая дополнительная степень свободы, которой не было у неё в парообразном состоянии, появилась в состоянии жидком?!
Для ртути теплоёмкость примерно одинакова, как для твёрдой, так для жидкой и парообразной фаз.
Для всех, подчёркиваю, для всех простых (одноатомных) в-в теплоёмкомкость примерно одинакова для всех агрегатных состояний, разумеется, только, если температура этих агрегатных состояний различается не на несколько сотен и больше градусов.
При низких температурах теплоёмкость плавно уменьшается, а при увеличении температуры плавно увеличивается.
А вот у сложных веществ, молекула которых состоит из нескольких атомов, теплоёмкость в жидкой фазе скачком увеличивается в разы, по сравнеию с другими фазами.
Сей факт современная наука стыдливо обходит молчанием.
На мой взгляд, объяснение этого феномена следует искать в строении вещества (строении молекулы).
Ну а поскольку современные представления о строении молекулы не дают возможности внятно и непротиворечиво объяснить феномен скачкообразного увеличения теплоёмкости сложных в-в в жидкой фазе, то есть все основания для сомнений в правильности существующих представлений о строении молекулы, да и молекулярно-кинетической теории тоже.
Автор: Тихомиров Евгений 8.12.2018, 17:17
ВСе теории неверны, иначе и быть не может.
Автор: mechanic 9.12.2018, 4:26
Автор: Digger 9.12.2018, 6:32
Существование ионов, как ионизированных атомов и молекул, конечно, же не отрицаю.
Ответьте на один мой простой вопрос, чтобы мы могли даигаться дальше:
Как объяснить скачкообразное увеличение теплоёмкости сложных в-в в жидкой фазе?
Автор: Метафизик 9.12.2018, 8:57
Вы сами-то никогда не задумывались над абсурдностью современных представлений о химической связи, образованной т.н. "валентными электронами".
Считается, что электроны - отрицательно заряжены, а из этого следует, что они не млгут спариваться, но только отталкиваться. Не химия, а какой-то гей-парад а Вашингтоне.
Давайте попробуем абстрагироваться от химических связей, и посмотреть на строение в-ва с другой стороны:
Вам наверняка известно, что углерод может существовать в трёх различных аллотропных модификациях: сажа, графит и алмаз.
За каким лешим электронам двух атомов углерода нужно спариваться, если атомы углерода и так электронейтральны?
Давайте попробуем посмотреть на строение молекул с другой стороны:
Поскольку Вы знаете и понимаете термодинамику, то Вас наверняка должен заинтересовать вопрос о том, почему теплоёмкость выше перечисленных аллотропных модификаций существенно различается.
Так, например, мольная теплоёмкость алмаза составляет примерно 6 Дж/моль*К, графита 8, а сажи 25 Дж/моль*К !
Любопытная получается картина: в алмазе самые прочные связи, т.е. на раскачку атома углерода в алмазе нужно затратить больше энергии, нежели в графите, и уж тем болеее в саже.
Но видим-то мы совсем иное!
Как,по-Вашему, можно объяснить сей неоспоримый факт?
Или другой пример:
Теплоёмкость воды в твёрдом (лёд) и газообразном (пар) агрегатном состоянии одинакова, а вот в жидкой фазе её теплоёмкость выше в 2,5 раза.
Вопрос: какая-такая дополнительная степень свободы, которой не было у неё в парообразном состоянии, появилась в состоянии жидком?!
Для ртути теплоёмкость примерно одинакова, как для твёрдой, так для жидкой и парообразной фаз.
Для всех, подчёркиваю, для всех простых (одноатомных) в-в теплоёмкомкость примерно одинакова для всех агрегатных состояний, разумеется, только, если температура этих агрегатных состояний различается не на несколько сотен и больше градусов.
При низких температурах теплоёмкость плавно уменьшается, а при увеличении температуры плавно увеличивается.
А вот у сложных веществ, молекула которых состоит из нескольких атомов, теплоёмкость в жидкой фазе скачком увеличивается в разы, по сравнеию с другими фазами.
Сей факт современная наука стыдливо обходит молчанием.
На мой взгляд, объяснение этого феномена следует искать в строении вещества (строении молекулы).
Ну а поскольку современные представления о строении молекулы не дают возможности внятно и непротиворечиво объяснить феномен скачкообразного увеличения теплоёмкости сложных в-в в жидкой фазе, то есть все основания для сомнений в правильности существующих представлений о строении молекулы, да и молекулярно-кинетической теории тоже.
Убедительно...
Автор: mechanic 11.12.2018, 7:25
Вы сами-то никогда не задумывались над абсурдностью современных представлений о химической связи, образованной т.н. "валентными электронами".
Считается, что электроны - отрицательно заряжены, а из этого следует, что они не млгут спариваться, но только отталкиваться. Не химия, а какой-то гей-парад а Вашингтоне. thumbsdown.gif
Ответьте на один мой простой вопрос, чтобы мы могли даигаться дальше:
Как объяснить скачкообразное увеличение теплоёмкости сложных в-в в жидкой фазе?
Вот я привел две цитаты Diggerа. Неужели вы не видите в них непоследовательности и противоречия? Если вы не отрицаете существования ионов и считаете абсурдностью химическую связь "валентными электронами" и утверждаете, что электроны как одинаково заряженные не могут спариваться, а только отталкиваться.
Тогда разберем, что такое ион и валентные электроны. Вот определение валентного электрона:
В химии валентными электронами называют электроны, находящиеся на внешней (валентной) оболочке атома.
А вот определение иона:
Ио́н (др.-греч. ἰόν «идущее») — частица, в которой общее число протонов не равно общему числу электронов. Ион, в котором общее число протонов больше общего числа электронов, имеет положительный заряд и называется катионом. Ион, в котором общее число протонов меньше общего числа электронов, имеет отрицательный заряд и называется анионом.
Как появляются ионы? Верхняя оболочка атома содержит так называемые валентные электроны, наименее связанные с ядром. В верхней оболочке число электронов не может превышать восьми. Восемь - наиболее устойчивая структура , присущая инертным газам. Если электронов во внешнем слое меньше 4х - атом под влиянием внешних сил может терять свои валентные электроны, превращаясь в положительно заряженный ион, а если более 4х- то принимать (захватывать) чужие электроны, превращаясь в отрицательно заряженный ион. При этом в каждом ионе создается устойчивый наружный слой, состоящий из 8 электронов. Разноименные ионы, например, Na+ и Cl- притягиваются образуя молекулу NaCl - поваренную соль с ионной связью Что же сложного я здесь написал? Это и есть САМОЕ ПРОСТОЕ образование молекул. Хотя атом хлористого натрия в целом представляет нейтральную молекулу, но система двух ионов является системой из двух зарядов , способной создавать электрическое поле. Два иона, притянувшихся друг к другу, обладают способностью электростатически взаимодействовать друг с другом и образовывать кристаллическую решетку. А вы полагаете , что молекулы это нейтральные шарики, сбившиеся в кучу. Это самое примитивное представление о строении твердого тела.
На самом деле твердые тела устроены гораздо сложнее. Ионная связь - простейшая из возможных. О ковалентной связи атомов в молекулах одного элемента я уже писал. Существует еще полярная ковалентная связь. Для пояснения ее необходимо приготовить рисунки, а пока я отвечу насчет теплоемкости. Вопрос объяснения теплоемкости различных веществ и фаз не является предметом термодинамики, так как целиком зависит от теорий строения вещества. Существует классическая теория теплоемкости твердых тел, основанная на молекулярной теории, которая правильно описывает определенный круг явлений, но многие явления она не объясняет по причине слишком упощенной модели, принятой в этой теории. Более точные результаты,согласующиеся с опытом дает квантовая теория. Подробнее читайте у Сивухина Курс Физики т.2 стр. 220-227.
Вот теперь и смотрите: кто идет от простого к сложному, а кто задает самый сложный вопрос о теплоемкости, на который у науки пока нет однозначного ответа для всех состояний вещества.
Автор: Digger 11.12.2018, 8:06
Тогда разберем, что такое ион и валентные электроны. Вот определение валентного электрона:
В химии валентными электронами называют электроны, находящиеся на внешней (валентной) оболочке атома.
А вот определение иона:
Ио́н (др.-греч. ἰόν «идущее») — частица, в которой общее число протонов не равно общему числу электронов. Ион, в котором общее число протонов больше общего числа электронов, имеет положительный заряд и называется катионом. Ион, в котором общее число протонов меньше общего числа электронов, имеет отрицательный заряд и называется анионом.
Как появляются ионы? Верхняя оболочка атома содержит так называемые валентные электроны, наименее связанные с ядром. В верхней оболочке число электронов не может превышать восьми. Восемь - наиболее устойчивая структура , присущая инертным газам. Если электронов во внешнем слое меньше 4х - атом под влиянием внешних сил может терять свои валентные электроны, превращаясь в положительно заряженный ион, а если более 4х- то принимать (захватывать) чужие электроны, превращаясь в отрицательно заряженный ион. При этом в каждом ионе создается устойчивый наружный слой, состоящий из 8 электронов. Разноименные ионы, например, Na+ и Cl- притягиваются образуя молекулу NaCl - поваренную соль с ионной связью Что же сложного я здесь написал? Это и есть САМОЕ ПРОСТОЕ образование молекул. Хотя атом хлористого натрия в целом представляет нейтральную молекулу, но система двух ионов является системой из двух зарядов , способной создавать электрическое поле. Два иона, притянувшихся друг к другу, обладают способностью электростатически взаимодействовать друг с другом и образовывать кристаллическую решетку. А вы полагаете , что молекулы это нейтральные шарики, сбившиеся в кучу. Это самое примитивное представление о строении твердого тела.
На самом деле твердые тела устроены гораздо сложнее. Ионная связь - простейшая из возможных. О ковалентной связи атомов в молекулах одного элемента я уже писал. Существует еще полярная ковалентная связь. Для пояснения ее необходимо приготовить рисунки, а пока я отвечу насчет теплоемкости. Вопрос объяснения теплоемкости различных веществ и фаз не является предметом термодинамики, так как целиком зависит от теорий строения вещества. Существует классическая теория теплоемкости твердых тел, основанная на молекулярной теории, которая правильно описывает определенный круг явлений, но многие явления она не объясняет по причине слишком упощенной модели, принятой в этой теории. Более точные результаты,согласующиеся с опытом дает квантовая теория. Подробнее читайте у Сивухина Курс Физики т.2 стр. 220-227.
Вот теперь и смотрите: кто идет от простого к сложному, а кто задает самый сложный вопрос о теплоемкости, на который у науки пока нет однозначного ответа для всех состояний вещества.
Один простой вопрос: как объяснить скачкообразное увеличение теплоёмкости сложных веществ при переходе из твёрдой или газовой фаз в фазу жидкую, и почему этот факт современная наука обходит молчанием?
Насколько понял, у Вас объяснения этому феномену нет.
А отсутствие объяснения - свидельство того, что в рамках существующих общепринятых представлений о строении в-ва внятное и непротиворечивое объяснение не может быть дано.
А коли так, то неверны существующие представления.
Следовательно, всё Вами и г-ном Сивухинным написанное - наукообразный трёп, поскольку вы оба считаете общепринятые представления о строении в-ва правильными.
"Блажен кто верует"
Автор: vps137 11.12.2018, 10:45
Насколько понял, у Вас объяснения этому феномену нет.
А отсутствие объяснения - свидельство того, что в рамках существующих общепринятых представлений о строении в-ва внятное и непротиворечивое объяснение не может быть дано.
А коли так, то неверны существующие представления.
Следовательно, всё Вами и г-ном Сивухинным написанное - наукообразный трёп, поскольку вы оба считаете общепринятые представления о строении в-ва правильными.
"Блажен кто верует"
Вы здесь немного всё попутали. Переходы, которые вы перечислили, - это фазовые переходы первого рода, а переходы, при которых скачком меняется теплоёмкость, - это переходы второго рода, напр. переход в сверхпроводящее состояние. Объяснений таким переходам - множество. Они изложены в специальной литературе по физике твёрдого тела, но теория, насколько я знаю, ещё далека до завершения. Эти теории либо слишком общие и тогда плохо объясняют конкретные случаи, либо слишком конкретные, феноменологические - объясняющие только какой-либо частный случай.
Я, работая в РАН, тоже занимался как мог объяснением одного интересного частного случая, мартенситного превращения в стали. Было написано три статьи, в которых предлагался новый механизм этого превращения, получен благоприятный отзыв из института кристаллографии, но местные царьки не дали возможности публиковать мои работы. Согласие с экспериментом было наилучшим среди всех других теорий. Имело смысл пробиваться дальше, чтобы в конце концов "остепениться", но тут началась Перестройка, фазовый переход на государственном уровне...
Автор: Digger 11.12.2018, 12:00
Это Вы всё перепутали: речь идёт не о филологии (названии того или иного феномена), а о факте, подтверждаемом измерением - скачкообразном увеличении теплоёмкости сложных веществ при переходе их из газовой и твёрдой фаз в фазу жидкую.
В чём принципиальное отличие фазового перехода "первого рода" от перехода "второго рода" с точки зрения физики?
Какая мне разница, как был выполнен переход из твёрдой или газовой фазы в жидкую, если физические свойства в-ва после перехода любого рода - одинаковы?
Меня не интересует переход, а свойство сложных в-в в жидкой фазе, а именно их экстремально высокую теплоёмкость (способность запасать тепловую энергию) в жидкой фазе.
Автор: vps137 11.12.2018, 12:44
В чём принципиальное отличие фазового перехода "первого рода" от перехода "второго рода" с точки зрения физики?
Какая мне разница, как был выполнен переход из твёрдой или газовой фазы в жидкую, если физические свойства в-ва после перехода любого рода - одинаковы?
Меня не интересует переход, а свойство сложных в-в в жидкой фазе, а именно их экстремально высокую теплоёмкость (способность запасать тепловую энергию) в жидкой фазе.
Как в чем отличие? Это же должно быть вам известно, если вы занимаетесь теплоёмкостью и всеми такими штуками.
В фазовых переходах первого рода меняется агрегатное состояние вещества, меняется объём и другие физические свойства, которые видны на глаз. При переходах второго рода меняются лишь некоторые неочевидные свойства - теплоёмкость, магнитные, электрические свойства. Напр. в мартенситном превращении меняется структура, решетка из гранецентрированной кубической переходит за микросекунды в объёмоцентрированную и наоборот. Поэтому то, что вы говорите, что вам нет разницы, может означать лишь то, что вы не пытаетесь разобраться в сути, а "сшибаете вершки", нагромождая всякий вздор в одну кучу, грубо говоря, занимаетесь болтологией и критиканством всех и вся. Вот это ваша истинная позиция варяга?
Могу, конечно, допустить редкую вероятность того, что в вашем лице мы имеем некоего самоучку, который задался целью сделать нечто вроде перпетум мобиле. В этом случае вероятность дать вам верный ответ также очень мала, потому что неизвестно чего вы добились и добились ли вообще.
Послушаем, что скажет заморский специалист, когда проснётся. Леонид, ау!
Автор: Digger 11.12.2018, 14:30
В фазовых переходах первого рода меняется агрегатное состояние вещества, меняется объём и другие физические свойства, которые видны на глаз. При переходах второго рода меняются лишь некоторые неочевидные свойства - теплоёмкость, магнитные, электрические свойства. Напр. в мартенситном превращении меняется структура, решетка из гранецентрированной кубической переходит за микросекунды в объёмоцентрированную и наоборот. Поэтому то, что вы говорите, что вам нет разницы, может означать лишь то, что вы не пытаетесь разобраться в сути, а "сшибаете вершки", нагромождая всякий вздор в одну кучу, грубо говоря, занимаетесь болтологией и критиканством всех и вся. Вот это ваша истинная позиция варяга?
Могу, конечно, допустить редкую вероятность того, что в вашем лице мы имеем некоего самоучку, который задался целью сделать нечто вроде перпетум мобиле. В этом случае вероятность дать вам верный ответ также очень мала, потому что неизвестно чего вы добились и добились ли вообще.
Послушаем, что скажет заморский специалист, когда проснётся. Леонид, ау!
Ещё раз: За каким лешим мне знать, каким способом был совершён переход от твёрдого тела или пара к жидкости, если свойства жидкости, полученной при этих переходах, одинаковы?
Зачем Вы занимаетесь болтологией, "наводя тень на плетень"?
Моё "критиканство" заключается во вскрытии противоречий существующих общепринятых теорий экспериментальным фактам.
А вот Ваша позиция, на мой взгляд, заключается в забалтывании неудобных вопросов.
Поиск истины и уход от трудных вопросов - вещи несовместимые.
Т.е. Ваша цель не поиск истины, а что-то иное.
Интересно, что же?
А что касается того, добился ли я чего-то своим "критиканством", то могу со всей ответственностью заявить, что смог найти внятное и непротиворечивое объяснение причине, по которой теплоёмкость аллотропных модификаций того же углерода, различна, почему одинаковые атомы углерода образуют сажу, графит и алмаз, почему объём занимаемый молекулой, состоящей из нескольких атомов не намного больше объёма, занимаемого каждым из атомов, входящих в состав молекулы, почему теплоёмкость сложных в-в в жидкой фазе экстремально высокая.
А это как раз те вопросы, на которые современная наука ответить не в состоянии.
Думаю, что и объяснение свойств мартенсита, которым Вы занимались, тоже будет найдено, если иходить из других представлений о строении молекулы, нежели из тех, которые насаждаются современной наукой.
Автор: mechanic 11.12.2018, 19:16
"Блажен кто верует"
Наукообразным трепом занимаетесь вы, потому как ничего не прочитав, сразу даете ответ, типа: " Доктора Живаго" (или Солженицына) не читал, но осуждаю. Строение газов хорошо известно и оно неплохо описывается МКТ даже в ее простейшем варианте. Структура кристаллических тел хорошо изучена физическими методами, прежде всего рентгеноструктурным анализом, ультразвуковыми и другими методами, вовсе не умозрительными построениями, как вы это себе представляете. Именно успехи в изучении строения вещества позволили синтезировать несуществующие в природе вещества, например на основе бора, кристаллическая решетка которого аналогична алмазу, а твердость выше , чем у алмаза. Точно также на основании знаний о структуре природного алмаза и графита удалось в 50х годах прошлого века получить из графита искусственные алмазы.
Жидкости и аморфные тела занимают промежуточное положение между газами и кристаллическими телами. В виду чисто технических трудностей они изучены в гораздо меньшей степени, чем твердые тела и газы. Этим и объясняется отсутствие теорий объясняющих их поведение во всех их состояниях.
Вы думаете , что трудности в науке легко преодолеть, сбросив по методу Остапа Бендера все шахматы с доски? Ошибаетесь. Для на чала объясните почему до сих пор нет удовлетворительной теории трения. Это вам ближе, здесь никакой "химии", в вульгарном смысле этого слова, нет.
Автор: vps137 11.12.2018, 19:17
Зачем Вы занимаетесь болтологией, "наводя тень на плетень"?
Вами ранее был задан
Теперь вы говорите, что переход вас не интересует. Но если нет фазового перехода, то нет и резкого изменения свойств. Тогда непонятно о чем речь.
Скажите просто и ясно что вас интересует и наука, может быть, не обойдёт вас молчанием.
Автор: Digger 11.12.2018, 19:39
Теперь вы говорите, что переход вас не интересует. Но если нет фазового перехода, то нет и резкого изменения свойств. Тогда непонятно о чем речь.
Скажите просто и ясно что вас интересует и наука, может быть, не обойдёт вас молчанием.
Можзет быть так будет понятнее: почему при фазовом преходе простых (одноатомных) в-в в жидкую фазу из твёрдой или газовой, не происходит резкого изменения теплоёмкости, как это происходит в случае со сложными в-вами?
Дело не в фазовом переходе, а в строении в-ва.
Неужели Вам это не понятно?!
Автор: vps137 12.12.2018, 3:28
Дело не в фазовом переходе, а в строении в-ва.
Неужели Вам это не понятно?!
Хорошо. Может быть, я уловил суть вашего вопроса.
Материалы со сложным составом допускают больше вариантов для строения своей структуры. Напр. атомы меньшего размера могут занимать при разных условиях разные положения относительно атомов больших размеров. Они более подвижны и поэтому изменение внешних условий сказывается на них сильнее. Теплоёмкость, как я понимаю, связана со способностью атомов колебаться в своей решетке. Среди себе подобных атомов варианты колебаний, т.н. моды, строго ограничены. Этим, возможно, и можно объяснить ваш факт.
Более полное объяснение, конечно, требует детального рассмотрения в рамках соответствующих разделов физики - физики твердого тела, термодинамики, квантовой механики и проч. с привлечением данных по исследованию состава, структуры и прочих свойств тех объектов, которые вам интересны. Таких данных теперь море для самых разных веществ.
Автор: Digger 12.12.2018, 4:30
Материалы со сложным составом допускают больше вариантов для строения своей структуры. Напр. атомы меньшего размера могут занимать при разных условиях разные положения относительно атомов больших размеров. Они более подвижны и поэтому изменение внешних условий сказывается на них сильнее. Теплоёмкость, как я понимаю, связана со способностью атомов колебаться в своей решетке. Среди себе подобных атомов варианты колебаний, т.н. моды, строго ограничены. Этим, возможно, и можно объяснить ваш факт.
Более полное объяснение, конечно, требует детального рассмотрения в рамках соответствующих разделов физики - физики твердого тела, термодинамики, квантовой механики и проч. с привлечением данных по исследованию состава, структуры и прочих свойств тех объектов, которые вам интересны. Таких данных теперь море для самых разных веществ.
Ну что же, я Вас тоже понял: Вы способны объяснить всё что угодно, не давая конкретного ответа на конкретный вопрос.
Почему среди себе подобных атомов варианты колебаний ограничены?
Ну, а уж квантовая "механика", и подавно, сможет "объяснить" любую небывальщину.
Автор: alal 12.12.2018, 8:50
http://files.school-collection.edu.ru/dlrstore/4a8731e1-0856-617e-d779-7c202fb4d5a6/00144678861340800/00144678861340800.htm
https://ru.coursera.org/lecture/physics-global-project/stiepieni-svobody-dvizhieniia-moliekul-zksN6
Автор: Digger 12.12.2018, 9:21
https://ru.coursera.org/lecture/physics-global-project/stiepieni-svobody-dvizhieniia-moliekul-zksN6
Вы, видимо, не читали начала дискуссии.
А вопрос, заданный в самом её начале, звучал так: "как объяснить экстремально высокую теплоёмкость сложных веществ в жидкой фазе по сравнению с газовой и твёрдой?
Какая такая дополнительна "степень свободы" появилась у молекулы жидкости, которой у неё не было в газовой и твёрдой фазах?"
Автор: mechanic 13.12.2018, 6:58
Коль зашла речь о степенях свободы, то потрудитесь прочесть страницы из курса физики Сивухина для университетов и МФТИ, на которые варяг ленится даже взглянуть.
[attachment=270:p0221.png] [attachment=271:p0222.png] [attachment=272:p0223.png] [attachment=273:p0224.png]
Автор: Digger 13.12.2018, 10:29
С лохотрономом, называемом "степени свободы", я разобрался ещё лет пятнадцать тому назад.
А вот вы продолжаете свято верить написанному в учебниках.
Ещё раз повторяю вопрос: какую-такую дополнительную степень свободы приобретают молекулы сложного вещества в жидкой фазе, которой у них не было в фазах твёрдой и газовой?
Автор: mechanic 14.12.2018, 2:57
А вот вы продолжаете свято верить написанному в учебниках. thumbsdown.gif
Ещё раз повторяю вопрос: какую-такую дополнительную степень свободы приобретают молекулы сложного вещества в жидкой фазе, которой у них не было в фазах твёрдой и газовой?
Если бы вы удосужились прочесть те практически 3 страницы из Сивухина, вы тупо не повторяли свой вопрос о дополнительной степени свободы, так как дело совсем не в ней.
Что касается теплоемкости жидкостей, вот что известно из курса Техническая термодинамика Кириллина. (стр. 148 и 149)
[attachment=274:p0148.png]
[attachment=275:p0149.png]
Автор: Digger 14.12.2018, 6:27
Что касается теплоемкости жидкостей, вот что известно из курса Техническая термодинамика Кириллина. (стр. 148 и 149)
[attachment=274:p0148.png]
Похоже, вы читаете не вникая в смысл написанного.
Ну как тут не вспомнить покойного Михаила Николаевича (вечная ему память).
http://http:"//www.youtube.com/watch?v=eY2PI4VG_j8"
Вот что написано у Кириллина:
"Что касается теплоемкости жидкости, то вследствие того, что удовлетворительная статистическая теория жидкости до сих пор не создана, какие-либо теоретические оценки величин ср и cv для жидкости (подобные, например, расчетам теплоемкости твердого тела по уравнению Дебая) не могут быть сделаны даже приближенно. Поэтому значения теплоемкости жидкости определяют или экспериментально, или расчетным путем с помощью термодинамических соотношений по значениям других".
Если расчёты теплоёмкости жидкости не могут быть сделаны даже приблизительно, в отличие от расчётов теплоёмкости твёрдого тела (подобно расчётам по уравнению Дебая), то это свидельствует о том, что у современной науки нет внятного и непротиворечивого объяснения феномену экстремально высокой теплоёмкости сложных в-в в жидкой фазе.
Т.е. Вы так и не ответили на мой вопрос о том "какая-такая "степень свободы" появляется у молекул сложных в-в в жидкой фазе, которой у них не было в фазах твёрдой или газовой?"
Автор: Patent 14.12.2018, 10:04
Пожалуйста, приведите этому конкретный пример.
Автор: ahedron 14.12.2018, 16:44
Интересно, что удельная теплоёмкость воды уже при 100оС уменьшается примерно в два раза...
Автор: Digger 14.12.2018, 17:34
Жидкая вода обладает значительной величиной массовой удельной теплоемкости, по сравнению с другими жидкостями. При атмосферном давлении и температуре до 100°С она находится в виде жидкости и ее теплоемкость изменяется в диапазоне от 4174 до 4220 Дж/(кг·град).
http://thermalinfo.ru/svojstva-zhidkostej/voda-i-rastvory/udelnaya-teploemkost-vody
Автор: mechanic 14.12.2018, 17:38
Да никакая! Взамодействие молекулы с близко расположеными соседями напоминает структуры, сходные с кристаллическими телами (ближний порядок), но с расположенными дальними молекулами такая связь не наблюдается и это сближает жидкость с газом. Рентгеноструктурный анализ дает размытую картину и подтверждает наличие близкого порядка. Детальное изучение жидкости связано с техническими трудностями. Этим и объясняется отсутствие удовлетворительной теории.
Автор: Digger 14.12.2018, 18:36
Это не технические трудности, а чисто психологические.
Броуновское движение обнаружено только в жидкостях, но ни в твёрдых телах, ни в газах оно экспериментально не обнаружено.
Теплоёмкость воды в газовой и твёрдой фазах одинакова. Именно, из-за наличия броуновского движения теплоёмкость жидкой воды аномально высока, по сравнению со льдом и паром.
Нет ни одного, подчёркиваю, ни одного! эксперимента, в котором бы было инструментально обнаружено броуновское (хаотическое) движение молекул газа при н.у.
Но ведь вы-то свято веруете, что молекулы газа хаотически мечутся, аки оглашенные.
А поэтому непротиворечивое объяснение аномально высокой теплоёмкости сложных в-в в жидкой фазе, в рамках существующих представлений о природе теплоты, не может быть найдено.
Автор: mechanic 14.12.2018, 19:07
Вы это должны доказать в отношении газов. Ссылочку - в студию. У меня другая информация https://ibrain.kz/fizika/brounovskoe-dvizhenie
Автор: ahedron 14.12.2018, 19:31
Потому что вода переходит в пар...
Автор: Digger 14.12.2018, 19:51
Во-первых, в физике не принято доказывать наличие отсутствия, но принято доказывать наличие присутствия, причём, доказывать экспериментально.
Во-вторых, ваша ссылка является беллетристикой, но, отнюдь, не экспериментальным док-вом.
С таким же успехом я могу вам привести пример, когда в сильно накуренной комнате дым слоями висит под потолком ("хоть топор вешай").
Поэтому, не сочтите за труд дать ссылку на инструментально измеренную скорость молекул газа газа при н.у.
Ждём-с.
Автор: alal 14.12.2018, 23:37
Нет ни одного, подчёркиваю, ни одного! эксперимента, в котором бы было инструментально обнаружено броуновское (хаотическое) движение молекул газа при н.у.
Но ведь вы-то свято веруете, что молекулы газа хаотически мечутся, аки оглашенные.
Сколько будут просить, столько будем давать ))
https://www.youtube.com/watch?v=3mnHd1_nqEs
Или вы не признаете Броуна и в жидкости и в газе, или признаете и там и там!
Другого доказательства броуновского движения не существует, молекулы не видимы, а что-то дергается без видимой причины
Решайте, что - черти, духи, вселенское трясение ?
Автор: mechanic 14.12.2018, 23:40
Ха-ха! Не принято доказывать, например, отсутствие воды и атмосферы на Луне? Можно и нужно! Отсутствие чего- либо не менее важно присутствия. Приведу пример. Многие врачи и специалисы - хреновы утверждают, что обычную водку нельзя считать глютен-фри, так как она изгототовлена из зерна, содержащего белок - клейковину. Эти болваны просто не понимают, что белок не переходит в спирт при перегонке, тем более многократной. Вот и приходится доказывать тем, кто прогуливал лекции по химии и физике и верят тем, кто эти предметы вообще не проходил (или проходил мимо).
Автор: Digger 15.12.2018, 8:17
Таким образом, вы не сумели представить экспериментального подтверждения основного положения МКТ, постулирующей хаотическое движение молекул газа при н.у. со сверхзвуковыми скоростями.
Т.е. МКТ не имеет надлежащего экспериментального обоснования, а, следовательно, не имеет права нзываться теорией. Поэтому МКТ следует переименовать в МКГ (молекулярно-кинетическую гипотезу).
Ч.Т.Д.
Автор: Patent 15.12.2018, 8:31
Цитата
Пожалуйста, приведите этому конкретный пример.
Открывая учебник физики и читаем: "Движение молекул в газах имеет беспорядочный характер: скорости молекул не имеют какого-либо преимущественного направления, а распределены хаотически по всем направлениям».
Это исходный и главный постулат МКТ. Из него следует, что невозможно предсказать - в какие стороны разлетятся молекулы после их столкновения.
Из него следует, что для каждой молекулы существует равновероятность дальнейшего движения по любому направлению. Именно поэтому согласно философской части МКТ считается, что молекулы газа, заключённые в некоем сосуде, могут в определённый, хоть и чрезвычайно редкий момент собраться в какой-либо одной его половине.
Теперь смотрим - как лихо "подтверждено" математически основное уравнение МКТ.
Изначально хаотичное движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений. В принципе, против этого возражений нет. Естественно, каждое направление можно привязать к трём взаимно перпендикулярным плоскостям, совпадающих с осями декартовой системы координат. Некорректность в следующем действии. Согласно МКТ в любой момент времени вдоль каждого из трёх направлений должно перемешаться ровно одна треть от всех молекул. Причем опять же ровно половина из них — в противоположную сторону. Следовательно, согласно основному уравнению МКТ, ровно одна шестая от всех молекул в каждое мгновение должна двигаться вдоль одного из шести направлений.
Возникает вопрос. Как именно это условие могут и должны выполнять сами молекулы, если направления их движения после отскоков от других непредсказуемы?
Автор: Patent 15.12.2018, 8:31
Цитата
Пожалуйста, приведите этому конкретный пример.
Открывая учебник физики и читаем: "Движение молекул в газах имеет беспорядочный характер: скорости молекул не имеют какого-либо преимущественного направления, а распределены хаотически по всем направлениям».
Это исходный и главный постулат МКТ. Из него следует, что невозможно предсказать - в какие стороны разлетятся молекулы после их столкновения.
Из него следует, что для каждой молекулы существует равновероятность дальнейшего движения по любому направлению. Именно поэтому согласно философской части МКТ считается, что молекулы газа, заключённые в некоем сосуде, могут в определённый, хоть и чрезвычайно редкий момент собраться в какой-либо одной его половине.
Теперь смотрим - как лихо "подтверждено" математически основное уравнение МКТ.
Изначально хаотичное движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений. В принципе, против этого возражений нет. Естественно, каждое направление можно привязать к трём взаимно перпендикулярным плоскостям, совпадающих с осями декартовой системы координат. Некорректность в следующем действии. Согласно МКТ в любой момент времени вдоль каждого из трёх направлений должно перемешаться ровно одна треть от всех молекул. Причем опять же ровно половина из них — в противоположную сторону. Следовательно, согласно основному уравнению МКТ, ровно одна шестая от всех молекул в каждое мгновение должна двигаться вдоль одного из шести направлений.
Возникает вопрос. Как именно это условие могут и должны выполнять сами молекулы, если направления их движения после отскоков от других непредсказуемы?
Автор: Digger 15.12.2018, 9:10
https://www.youtube.com/watch?v=3mnHd1_nqEs
Или вы не признаете Броуна и в жидкости и в газе, или признаете и там и там!
Другого доказательства броуновского движения не существует, молекулы не видимы, а что-то дергается без видимой причины
Решайте, что - черти, духи, вселенское трясение ?
Э, любезный, это ваше "доказательство", доказательством не является.
Во-первых, поскольку в приведённом вами видео нет инструментальных измерений, а, во-вторых, само по себе, наблюдение не может считаться экспериментом.
Поскольку эксперимент, по определению, есть взаимодействие с исследуемым объектом в управляемых условиях, позволяющее установить причинно-следственные связи.
Т.к. причина броуновского движения современной наукой не установлена, то ни о каком экспериментальном подтверждении МКТ и речи быть не может.
А причиной всякого физического процесса, как известно, являются силы.
Между атомами и молекулами действуют т.н. "силы Ван дер Ваальса".
Силы эти зависят от температуры.
Т.е. они-то и являются причиной броуновского движения.
Движение молекулы жидкости в непрерывной и несжимаемой среде возможно только в случае силового воздействия на неё со стороны соседних молекул.
Можно преположить, что броуновское движение молекулы жидкости напоминает выстрел вишнёвой косточки, зажатой между двух пальцев.
Но в таком случае становится очевидным, что само броуновское движение не является носителем тепловой энергии тел, но служит лишь индикатором тепловой накачки атомов и молекул, как самостоятельных колебательных систем, способных поглощать и излучать тепловую энергию.
Или, иначе говоря, тепловая энергия - это не кинетическая энергия атомов и молекул, а энергия колебательных систем, коими, несомненно, являются атомы и молекулы.
Так ШтА, никаких чертей, духов, и никакого вселенского трясения.
Разумеется, если перестать верить МКТ.
Автор: alal 15.12.2018, 20:20
Во-первых, поскольку в приведённом вами видео нет инструментальных измерений, а, во-вторых, само по себе, наблюдение не может считаться экспериментом.
Поскольку эксперимент, по определению, есть взаимодействие с исследуемым объектом в управляемых условиях, позволяющее установить причинно-следственные связи.
Т.к. причина броуновского движения современной наукой не установлена, то ни о каком экспериментальном подтверждении МКТ и речи быть не может.
А причиной всякого физического процесса, как известно, являются силы.
Между атомами и молекулами действуют т.н. "силы Ван дер Ваальса".
Силы эти зависят от температуры.
Т.е. они-то и являются причиной броуновского движения.
Движение молекулы жидкости в непрерывной и несжимаемой среде возможно только в случае силового воздействия на неё со стороны соседних молекул.
Можно преположить, что броуновское движение молекулы жидкости напоминает выстрел вишнёвой косточки, зажатой между двух пальцев.
Но в таком случае становится очевидным, что само броуновское движение не является носителем тепловой энергии тел, но служит лишь индикатором тепловой накачки атомов и молекул, как самостоятельных колебательных систем, способных поглощать и излучать тепловую энергию.
Или, иначе говоря, тепловая энергия - это не кинетическая энергия атомов и молекул, а энергия колебательных систем, коими, несомненно, являются атомы и молекулы.
Так ШтА, никаких чертей, духов, и никакого вселенского трясения.
Разумеется, если перестать верить МКТ.
Какие вишни? Какие абрикосы?
Если бы была показана любая часть вышеприведенного видео раздельно для газа и жидкости без поясняющей подписи, то почти невозможно отличить, где газ, а где жидкость.
Разумно предположить, что природа явлений одна, без всяких нагромаждений фантазий о косточкох и арбузах
Но если цель - показать свою креативную мощь и филологические способности (что полюбляют современные "эффективные манагеры"), то конечно, вперед !
Автор: Digger 15.12.2018, 22:10
Если бы была показана любая часть вышеприведенного видео раздельно для газа и жидкости без поясняющей подписи, то почти невозможно отличить, где газ, а где жидкость.
Разумно предположить, что природа явлений одна, без всяких нагромаждений фантазий о косточкох и арбузах
Но если цель - показать свою креативную мощь и филологические способности (что полюбляют современные "эффективные манагеры"), то конечно, вперед !
Если вам угодно верить в чертей, духов и вселенское трясение, то флаг вам в руки.
Если ваша цель защищать абсурдную теорию, не дающую ответов ни на вопрос о причине броуновского движения, ни о механизме теплового излучения, ни о феномене аномально высокой теплоёмкости сложных в-в в жидкой фазе, неспособной рассчитать теплоёмкость, теплопроводность и диффузию, то это ваш выбор.
Автор: mechanic 17.12.2018, 6:59
Ч.Т.Д.
Экспериментальное обоснование МКТ для газов было создано задолго до ее создания. Это опыты Бойля, Мариотта, Шарля и Гей-Люссака, а также обобщение выведенных ими эмпирических газовых законов Клапейроном и Менделеевым. Почему только для газов, я уже говорил, но вы до сих пор не поняли. Исходные предпосылки МКТ в ее простейшей редакции состоят в том, что размерами молекул (атомов) можно пренебречь по сравнению со средними расстояниями между
ними, а также можно пренебречь силами их взаимного притяжения на этих расстояниях. Даже ежику под газом должно быть ясно, что этим предпосылкам может удовлетворять только газообразное состояние вещества. В твердом и жидком состояниях веществ указанные условия не соблюдаются, поэтому с МКТ для этих состояний взятки - гладки. Нужна более общая теория. Более точным, чем уравнение Клапейрона, являются эмпирические и полуэмпирические уравнения, которых насчитывается не один десяток, из которых наиболее простым и понятным является уравнение Ван-дер-Ваальса. В него, по сравнению с уравнением Клапейрона, внесены две поправки. Одна из них учитывает размеры атомов или молекул, другая - силы их взаимодействия, а именно, - силы притяжения на определенных расстояниях без раскрытия природы этих сил в каждом конкретном случае. Эти силы называют Ван-дер- Ваальсовскими, но это никакие не особые силы, а просто силы существующие по факту. Природа и механизм возникновения этих сил могут быть различными в зависимости от строения вещества не только на атомно- молекулярном уровне, но и на внутриядерном.
Автор: vps137 17.12.2018, 7:54
ними, а также можно пренебречь силами их взаимного притяжения на этих расстояниях. Даже ежику под газом должно быть ясно, что этим предпосылкам может удовлетворять только газообразное состояние вещества. В твердом и жидком состояниях веществ указанные условия не соблюдаются, поэтому с МКТ для этих состояний взятки - гладки. Нужна более общая теория. Более точным, чем уравнение Клапейрона, являются эмпирические и полуэмпирические уравнения, которых насчитывается не один десяток, из которых наиболее простым и понятным является уравнение Ван-дер-Ваальса. В него, по сравнению с уравнением Клапейрона, внесены две поправки. Одна из них учитывает размеры атомов или молекул, другая - силы их взаимодействия, а именно, - силы притяжения на определенных расстояниях без раскрытия природы этих сил в каждом конкретном случае. Эти силы называют Ван-дер- Ваальсовскими, но это никакие не особые силы, а просто силы существующие по факту. Природа и механизм возникновения этих сил могут быть различными в зависимости от строения вещества не только на атомно- молекулярном уровне, но и на внутриядерном.
Варягу этого мало. Он хочет избавить человечество от веры в МКТ.
Автор: Patent 17.12.2018, 7:55
ними, а также можно пренебречь силами их взаимного притяжения на этих расстояниях. Даже ежику под газом должно быть ясно, что этим предпосылкам может удовлетворять только газообразное состояние вещества. В твердом и жидком состояниях веществ указанные условия не соблюдаются, поэтому с МКТ для этих состояний взятки - гладки. Нужна более общая теория. Более точным, чем уравнение Клапейрона, являются эмпирические и полуэмпирические уравнения, которых насчитывается не один десяток, из которых наиболее простым и понятным является уравнение Ван-дер-Ваальса. В него, по сравнению с уравнением Клапейрона, внесены две поправки. Одна из них учитывает размеры атомов или молекул, другая - силы их взаимодействия, а именно, - силы притяжения на определенных расстояниях без раскрытия природы этих сил в каждом конкретном случае. Эти силы называют Ван-дер- Ваальсовскими, но это никакие не особые силы, а просто силы существующие по факту. Природа и механизм возникновения этих сил могут быть различными в зависимости от строения вещества не только на атомно- молекулярном уровне, но и на внутриядерном.
НЕ НАДО МНОГО ПАФОСНЫХ СЛОВ.
Вы способны конкретикой подкрепить свои утверждения?
Тогда ответьте на мой конкретный вопрос.
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164699
Автор: Digger 17.12.2018, 8:53
ними, а также можно пренебречь силами их взаимного притяжения на этих расстояниях. Даже ежику под газом должно быть ясно, что этим предпосылкам может удовлетворять только газообразное состояние вещества. В твердом и жидком состояниях веществ указанные условия не соблюдаются, поэтому с МКТ для этих состояний взятки - гладки. Нужна более общая теория. Более точным, чем уравнение Клапейрона, являются эмпирические и полуэмпирические уравнения, которых насчитывается не один десяток, из которых наиболее простым и понятным является уравнение Ван-дер-Ваальса. В него, по сравнению с уравнением Клапейрона, внесены две поправки. Одна из них учитывает размеры атомов или молекул, другая - силы их взаимодействия, а именно, - силы притяжения на определенных расстояниях без раскрытия природы этих сил в каждом конкретном случае. Эти силы называют Ван-дер- Ваальсовскими, но это никакие не особые силы, а просто силы существующие по факту. Природа и механизм возникновения этих сил могут быть различными в зависимости от строения вещества не только на атомно- молекулярном уровне, но и на внутриядерном.
Это в каких-таких опытах, задолго до создания МКТ, или когда-нибудь после её создания, были измерены скорости молекул газа при н.у.?!
Разве вы не знаете, что скорости эти были постулированы ("притянуты за уши"), чтобы получить механистическое объяснение создаваемому газами давлению на стенки сосуда?
Вас неоднократно спрашивали на что расходуется работа, совершаемая опускающимся поршнем, сжимающим газ?
Скорости молекул газа увеличиваются при таком сжатии незначительно, а вот температура может вырасти весьма заметно.
Если вам когда-нибудь доводилось накачивать шины велосипеда ручным насосом, то вы это должны хорошо знать.
Т.е. МКТ даже здесь, казалось бы в чисто механическом процессе, оказывается бессильной.
Чего уж тогда говорить, что примитивные механистические представления, лежащие в фундаменте свременной теории теплоты, не способны объяснить ни механизм теплового излучения, ни аномально высокую теплоёмкость сложных веществ в жидкой фазе, ни рассчитать ни теплопроводность, ни теплоёмкость и даже диффузию.
Только не нужно врать, что МКТ имеет отношение только к газам, и не имеет к твёрдым телам и жидкостям.
МКТ была создана для объяснения природы газов, но и для объяснения теплоты.
МКТ - гипотеза являющаяся фундаментом современных представлений о теплоте, и постулирующая теплоту, как кинетическую энергию движущихся атомов и молекул, имеет прямое отношение к любым физическим процессам, касающихся теплоты.
Ну что же ещё нужно показать, где современная теория теплоты бессильна, чтобы доказать, что МКТ неверна в своей основе?!
Или для вас законы Бойля-Мариотта и Шарля, являются необходимым и достаточным доказательством справедливости МКТ, а на всё остальное, что прямо ей противоречит, нужно закрыть глаза?!
Почему в связи со вновь открывшимися обстоятельствами (существованием сил Ван дер Ваалься), открытыми в 20-м веке, МКТ не была подвергнута критическому переосмыслению?
Ведь силами отталкивания между молекулами может быть объяснена природа газов и механизм давления, оказываемого ими на стенки сосуда, т.е. то, что "объясняет" МКТ.
Отказ от МКТ позволит понять механизм теплового излучения и многое другое, чего МКТ объяснить не может в принципе.
Но вы упорно цепляетесь за примитивную механистическую гипотезу, упорно не желая видеть её бессилия в объяснении физических процессов, связанных с теплотой.
Автор: mechanic 19.12.2018, 7:42
С чего вы взяли, что открылись какие-то новые остоятельства и обнаружилось существование сил Ван-дер - Ваальса? МКТ разработала теоретическую модель идеального газа, в которой силы взаимного притяжения не учитываются в виду их малости. Не учитываются и размеры самих молекул в виду их малых размеров по сравнению со средними расстояниями между молекулами. Ван-дер- Ваальс никаких новых сил не открыл. Он изучал поведение реальных газов и ввел поправки к уравнению Клапейрона, учитывающие размеры молекул и силы их взаимного притяжения безотносительно к природе этих сил. Это потом уже эти силы назвали Ван- дер- Ваальсовскими. Уравнение Ван-дер- Ваальса более точно описывает состояние газов в зоне близкой к конденсации и качественно описывает процесс перехода газа в жидкое состояние. Это одно из десятков аналогичных уравнений, описывающих состояние реальных газов, причем не самое точное, но наиболее простое и понятное. Так что надо в МКТ переосмысливать? Точного уравнения состояния реальных газов нет, а эмпирические уравнения ничего нового в теорию не добавляют. Они просто используются в технических расчетах. Не проясняют они и природу сил молекулярного притяжения.
δA= P (V, T) dV
В уравнении работы давление является функцией двух переменных - объема и температуры. Без указания вида процесса решение не может быть определенным. В общем случае работа, производимая над системой (работа сжатия) расходуется на повышение ее внутренней энергии dU, параметрами которой являются давление, объем и температура.
МКТ - гипотеза являющаяся фундаментом современных представлений о теплоте, и постулирующая теплоту, как кинетическую энергию движущихся атомов и молекул, имеет прямое отношение к любым физическим процессам, касающихся теплоты.
Здесь неверным является то, что кинетическая теория имеет прямое отношение к любым физическим процессам. У нее есть ограничения, не позволяющие это сделать. Она не может объяснять процессы, происходящие на внутриатомном уровне, например, тепловое излучение.
Автор: Digger 19.12.2018, 9:33
Ложь, звиздёжь и провокация.
МКТ строилась на примитивном механистическом предположении, о том, что молекулы газа являются абсолютно упругими шариками, взаимодействующими только в момент соударения, аки бильярдные шары.
Но, как оказалось впоследствии, это не совсем так, и поэтому стали говорить об идеальных (не существующих) газах, строго подчиняющихся уравнениям МКТ и о газах реальных, которые только с некоторым приближением подчиняются этим законам, т.е. молекулы реального газа не являются абсолютно упругими шариками.
δA= P (V, T) dV
В уравнении работы давление является функцией двух переменных - объема и температуры. Без указания вида процесса решение не может быть определенным. В общем случае работа, производимая над системой (работа сжатия) расходуется на повышение ее внутренней энергии dU, параметрами которой являются давление, объем и температура.
Вот это и называется - "наводить тень на плетень". Вам чётко был оговорен процесс - процесс накачивания велосипедной шины ручным насосом и сопровождающий этот процесс нагрев корпуса насоса.
Скорость движения поршня насоса ок. 1 м/сек, а после нескольких качков корпус насоса начинает обжигать ладони рук. Скорость молекул газа под поршнем должна была увеличиться примерно на 2 м/сек, т.е. на доли процента, а температура-то выросла в разы.
Где деньги, Зин?!
Опять двадцать пять! Если по существующей теории (МКТ) вся тепловая энергия газа - это сумма кинетических энергий атомов и молекул, то откуда берётся энергия теплового излучения?
Между соударениями молекулы газа излучать не могут в принципе, поскольку, во-первых, электрически нейтральны, а, во-вторых, движутся равномерно и прямолинейно, а, в момент соударения тоже излучать не могут, поскольку соударение по МКТ абсолютно упругое, т.е. происходит без потерь.
Да и как хаотически мечущиеся молекулы, вообще, могут согласованно излучать?!
ведь тепловое излучение процесс гармонический, а не хаотический.
Поскольку МКТ, да и любая другая теория, будь-то квантовая, или статистическая не в состоянии объяснить механизм теплового излучения, то это свидельствует о том, что без отказа от МКТ такое объяснение невозможно получить в принципе.
Но разве можно признать МКТ неверной, если к её созданию приложили руку Максвелл, Клаузиус, Больцман, Шарль, Бойль, Мариотт и даже "великий" Эйнштейн?!
Покуда современной наукой не будет объяснён механизм теплового излучения, до тех пор наши представления о теплоте будут не знанием, а верой - верой в непогрешимость авторитетов.
А вера - это не наука, а мракобесие.
Без отказа от МКТ мы не сможем рассчитывать ни теплоёмкость, ни теплопроводность, ни диффузию.
Автор: Patent 19.12.2018, 12:11
Вы за свои слова способны отвечать?
Сколько можно от Вас ждать объяснений?
Здесь:
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164622
Вы указали, что «Строение газов хорошо известно и оно неплохо описывается МКТ даже в ее простейшем варианте».
Здесь:
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164686
на мой запрос о конкретном примере сослались на «Теоретический вывод уравнения Клапейрона».
Здесь:
http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164699
По этому поводу я Вам задал конкретный вопрос.
Вы намерены обосновывать своё утверждение ВНЯТНЫМ ответом на мой вопрос?
Или и дальше будете игнорировать неудобные вопросы и оперировать то лозунгами во славу МКТ, то невнятным отходом от неё?
Речь идёт о том, НАСКОЛЬКО ХОРОШО МКТ описывает газы.
И насколько корректно произвели привязку МКТ к эмпирически найденной зависимости.
Автор: mechanic 19.12.2018, 19:21
Изначально хаотичное движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений. В принципе, против этого возражений нет. Естественно, каждое направление можно привязать к трём взаимно перпендикулярным плоскостям, совпадающих с осями декартовой системы координат. Некорректность в следующем действии. Согласно МКТ в любой момент времени вдоль каждого из трёх направлений должно перемешаться ровно одна треть от всех молекул. Причем опять же ровно половина из них — в противоположную сторону. Следовательно, согласно основному уравнению МКТ, ровно одна шестая от всех молекул в каждое мгновение должна двигаться вдоль одного из шести направлений.
Возникает вопрос. Как именно это условие могут и должны выполнять сами молекулы, если направления их движения после отскоков от других непредсказуемы?
Во- первых, любой вектор то ли скорости, то ли силы можно разложить по трем взаимно перпендикулярным направлениям и иметь дело с проекциями этих векторов независимо от того есть увас возражения по этому поводу или нет. Теперь насчет РОВНО. МКТ- статистическая теория, где слово РОВНО места не имеет. Можно говорить о большинстве, подавляющем большинстве и бесконечно малом отклонении. Бессмысленно в статистике говорить о поведении одной молекулы, десятка, сотни и даже тысячи молекул. Молекулы , движущиеся хаотически сталкиваются между собой и при их столкновениях энергия и импульсы их выравниваются и приближаются к средним значениям, согласно максвелловскому распределению. Если речь идет о сосуде, вмещающем, скажем, 1 моль газа, содержащем 6,0222310^23 молекул, то вероятность того, что молекулы соберутся в одной части сосуда теоретически существует, но время такого события может наступить через миллиарды лет. Вы же не опасаетесь того, что, теоретически, все молекулы вашего тела могут двинуться в одном направлении и вы взлетите как ракета, потому что вероятность такого события может превысить время существования нашей Вселенной.
И насколько корректно произвели привязку МКТ к эмпирически найденной зависимости.
МКТ описывает ТОЧНО состояние идеальных газов. Все газы при температурах выше критической и не слишко высоких давлениях с достаточно высокой точностью можно считать идеальными и пользоваться для расчетов уравнением Клапейрона. Собственно газами следует называть перегретые пары. Пары допускают отклонения от идеальности и тем большие, чем они приближены к насыщению. Насыщенный пар и жидкое состояние уравнением Клапейрона вообще не описываются. Уравнение Ван-дер-Ваальса вовсе не эмпирическая зависимость, а уточнение уравнения Клапейрона для реальных газов. Вывод его и принятые допущения читайте https://ru.wikipedia.org/wiki/%D0%A3%D1%80%D0%B0%D0%B2%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5_%D0%92%D0%B0%D0%BD-%D0%B4%D0%B5%D1%80-%D0%92%D0%B0%D0%B0%D0%BB%D1%8C%D1%81%D0%B0
Автор: Patent 20.12.2018, 17:45
Именно к этому у меня возражений нет. И не было!
Не надо притягивать к своему пространственному ответу то, о чём не спрашивается.
А если в исходные данные для статистического подсчёта закладывается именно то, что РОВНО?
Что значит – «энергия и импульсы их выравниваются»?
Если это утверждение, а не пустая декларация, то этому должны быть внятные обоснования.
Они есть?
С этим доводом я знаком. Он может испугать и удовлетворить только тех, кто далее не задумывается.
У меня здесь - http://sopoviuriy.narod.ru/kniga.doc
На стр. 16 – 22 представлен разбор выпадений вариантов. На конкретном примере, хоть и малым количеством элементов, показана общая тенденция.
Ситуация такова, что сколько бы не было молекул в сосуде, а равномерных выпадений (согласно статистики) будет намного меньше, чем неравномерных.
Да! Они будут чередоваться. Но это не довод для того, чтобы утверждать, что в итоге за многие годы у миллионов обычных воздушных шариков никогда не может спонтанно появиться где-то вмятина, где-то бугорок.
Кроме того, речь получается идёт о том, что по МКТ по каким-то причинам именно пограничные со стенками молекулы постоянно распределены с абсолютной равномерностью. Возьмите в качестве исследуемого объёма именно приграничную область к круговой стенке воздушного шарика толщиной 0,1 мм. Для молекул в сопоставлении это очень большой объём. И далее непредвзято поразмышляйте - из каких данных, при заданном хаосе в рассматриваемой области, молекулы по МКТ обязаны удерживать оболочку в непоколебимом виде.
Если этот довод считаете убийственным, то это он таковой для Вас.
По указанной ссылке взгляните на рисунки и текст нем на стр. 10-12.
Там сопоставляется работа с тем, что при полной аналогии почему-то по МКТ работа не производится. Хотя также статической силе противостоит система в динамике.
А теперь честно сопоставьте, если по ТТЭ в воздушном шарике статической силе снаружи противостоит статическая сила изнутри, то это лучший вариант или нет?
Вот на ОСНОВАНИИ для этого вывода и сосредоточьтесь.
На чём именно основан это вывод? И насколько он корректен?
Вы петляете как заяц. Берём опять воздушный шарик. Смотрим на него и думаем – а если применять не идеальный газ, а реальный, то что в нём должно происходить и откуда молекулы внутри берут столько энергии, что бы противостоять и наружному давлению и ещё и оболочке стремящейся сжаться. Есть внятное объяснение этому?
Автор: mechanic 21.12.2018, 23:41
Если это утверждение, а не пустая декларация, то этому должны быть внятные обоснования.
Здесь я не точно выразился. Не скорости частиц их энергия и импульсы становятся равными, а термодинамическая система приходит в состояние равновесия. С точки зрения статистики распределение скоростей устаканивается и принимает вид распределения Максвелла. Большинство молекул будут иметь скорости, а стало быть импульсы и энергию близкую к средним величинам. Когда число частиц становится огромным, то влияние флуктуаций (отклонение от средних величин) практически сводится к нулю. В этом смысле и говорится о равномерном распределении скоростей молекул по степеням свободы.
Вам не нравится вывод, приведенный во всех учебниках, кроме школьных? Напишите ваши возражения по существу.
Что за вопрос невнятный? Любой газ в определенных условиях, например, в разреженном состоянии и при высокой температуре, ведет себя как идеальный, то есть следует с достаточной точностью уравнению Клапейрона. В других условиях - при повышенных давлениях и более низких температурах, он отклоняется от законов идеального газа и точнее следует уравнению Вандер- Ваальса либо другим уравнениям реальных газов. Если ваш воздушный шарик будет заполнен водяным паром, то при нуле градусов по Цельсию он начнет схлопываться по мере конденсации пара.
Вот здесь требуется уточнение: работа чего и какая работа. Потому что работа - работе рознь. Да и сам термин работа относится в термодинамике к двум разным вещам. Ведите разговор грамотно, в соответствии с принятой научной терминологией.
Автор: Patent 22.12.2018, 12:37
Цитаты:
Mechanic: МКТ описывает ТОЧНО состояние идеальных газов. Все газы при температурах выше критической и не слишко высоких давлениях с достаточно высокой точностью можно считать идеальными и пользоваться для расчетов уравнением Клапейрона.
Патент: Вот на ОСНОВАНИИ для этого вывода и сосредоточьтесь.
На чём именно основан это вывод? И насколько он корректен?
Мне непонятен принцип того, на основании чего указывается принадлежность к ИДЕАЛЬНОМУ газу. Какие конкретно факторы к этому приводят?
Если Вы на это ссылаетесь, то это указывает на то, что Вам это понятно. Можете здесь своими словами внятно это объяснить. Если своими словами не получается, то это указывает на то, что Вы запомнили вывод без понимания его происхождения. Я прав?
Если поняли, то делаю акцент на сути спрашиваемого.
Чем высокое давление влияет на именно характер ударов молекул по МКТ? Если только частотой, то мне именно это и непонятно. Как просто смена (увеличение или уменьшение) частоты ударов по МКТ меняет характеристику этих самых ударов?
Вот о конкретных причинах этого заявления и вопросы выше.
Патент:
Опять заячий прыжок подальше от ответа.
Здесь - http://sopoviuriy.narod.ru/kniga.doc
на стр. 10-12. Представлены рисунки и текст к ним.
И ответьте на конкретные вопросы.
В случае с установкой стреляющей шариками по плите, стремящейся опуститься под действием гравитации, работа производиться?
В случае с молекулами, удерживающими резиновую оболочку шарика стремящуюся сжаться, работа производится?
Автор: mechanic 25.12.2018, 7:08
Если Вы на это ссылаетесь, то это указывает на то, что Вам это понятно. Можете здесь своими словами внятно это объяснить. Если своими словами не получается, то это указывает на то, что Вы запомнили вывод без понимания его происхождения. Я прав?
Я начну с конца, но не этого вопроса, а с конца вашей книги на 82х страницах. В конце, как обычно, приводится перечень использованной литературы. Вот он:
1. «Элементарный учебник физики». Под ред. Ландсберга Г.С. Т.1, М., «Наука», 1985г.
2. «Элементарный учебник физики». Под ред. Ландсберга Г.С. Т.3, М., «Наука», 1986г.
3. «Молекулярная физика». И.К.Кикоин, А.К.Кикоин. М.,1963г.
4. «Уравнения состояния реальных газов», Вукалович М.П. и Новиков И.И. М., 1948г.
5. «Курс общей физики». Савельев И.В. М., Наука. Т 3. 1987г.
6. «Физика» 10 класс Г.Я. Мякишев; Б.Б.Буховцев 1990г
7. Г. Линдер «Картины современной физики», М., «Мир», 1977г
8. Л.Эллиот и Уилкокс «Физика» М. Изд. «Наука» 1975г.
9. М. Яворский и Ю. Селезнёв «Справочное руководство по физике» М., «Наука» 1989г
10. Эйнштейн, А. Инфельд, Л. Эволюция физики. В сборнике А.Эйнштейн «Эволюция физики». М. Устойчивый мир. 2001
11 А. Эйнштейн. Физика и реальность. М.: Наука, 1965г.,
12. «Политехнический словарь» Издательство «Советская энциклопедия»; М; 1977г.
13. «Физика» 6-7кл. А.В. Пёрышкин; Н.А. Родина.М. «Просвещение» 1985г.
14. «Физика» 8кл. А.В. Пёрышкин; Н.А. Родина.М. «Просвещение» 1989г
Это о чем -то говорит. На каком уровне можно дискутировать, если в этом перечне за единственным исключением (Курс физики Савельева) представлены школьные учебники, а также популярные и справочные издания? А самое главное - в нем нет и в помине ни одного учебника и, вообще, ни одной книги по термодинамике, не говоря уже о статистической физики , понимание которой требует знаний математики в объеме физмата университета.
О чем тогда дискутировать , если надо изучать термодинамику с нуля. Кстати, в курсе физики Савельева, вопросы, касающиеся термодинамики, изложены конспективно и, на мой взгляд, из рук вон плохо, так как не даются определения основных понятий.
Теперь отвечаю на заданный вопрос. Для того чтобы указать "принадлежность" реального газа к идеальному, на до прежде всего знать определение идеального газа в термодинамике, а не в статистике (МКТ).
Открываем для простоты поиска Википедию, статью "Газ" подраздел "Частные случаи":
(Выделено мной). Кстати, это моя правка статьи. (Ник - Thermokon). А дальше - проще простого . Если газ имеет температуру выше критической и прелестнительно невысокое давление (практически меньше) 200 атм., то отклонение его поведения от уравнения Клапейрона будет незначительным и такой газ можно считать идеальным для большинства технических расчетов. Для более грубых расчетов температура газа может быть и ниже критической, но значительно выше температуры конденсации. Все зависит от соотношения температуры и давления. Чем выше температура и ниже давление, тем более идеальным будет реальный газ. Это опытные факты, открытые Бойлем, Шарлем, Гей- Люссаком. Я внятно объяснил с точки зрения термодинамики?
Вот о конкретных причинах этого заявления и вопросы выше.
Если вас интересует статисический взгляд, то при разрежении, то есть при увеличении удельного объема, расстояния между молекулами увеличиваются по отношению к размерам молекул, поэтому размерами молекул и силами их притяжения можно пренебречь. Это и есть необходимые предпосылки для вывода уравнения идеального газа теоретическим путем. Вот тут оба подхода макроскопичесий и микроскопический дают сходные результаты.
Опять заячий прыжок подальше от ответа.
Вы сначала дайте мне ответ , что вы понимаете под работой и заодно - теплотой. А потом я вам постараюсь ответить совершается работа или нет. Иначе дело не пойдет.
Автор: Patent 26.12.2018, 11:37
Это о чем -то говорит. На каком уровне можно дискутировать, если в этом перечне за единственным исключением (Курс физики Савельева) представлены школьные учебники, а также популярные и справочные издания?
Мы сейчас здесь разбираем именно школьный курс.
Про то, что в школе относят к процессу РАБОТА.
Во-первых, при чём здесь моё понимание, если спрашивается о Вашем?
Понимание работы даётся в школьных учебниках.
Вам школьные трактовки для объяснений не подходят? Если не согласны со школьными трактовками, то дайте свои из …
Вам лучше знать - где Вы их берёте, поскольку они Ваши.
Давайте поэтапно.
Вот со своей позиции (а не с моего понимания) работы и теплоты и дайте по двум примерам чёткий ответ.
Пример 1. Установка стреляет шариками в плиту, которая установлена в вертикальных направляющих и под действием силы своей тяжести стремиться опуститься. Но это ей сделать не позволяют шарики, которыми снизу по ней стреляет соответствующая установка.
В этом случае плита совершает малые вертикальные перемещения. Чуть опуститься вниз, а после удара очередного шарика, опять сдвинется вверх. И так постоянно.
Вывод. Установка, посредством шариков совершает работу, периодически сдвигая вверх плиту.
Можно по-другому. Каждый шарик выполняет работу по перемещению плиты вверх не некую величину, отдавая ей часть своей кинетической энергии.
Пример 2. Рассматриваем фрагмент оболочки обычного воздушного шарика.
Шарик находится в условиях, когда температура внутри шарика и снаружи едина.
Рассматриваем то, что получается при этих условиях по МКТ.
Растянутая оболочка шарика стремиться сжаться. В этом случае стремление каждого фрагмента оболочки переместиться к центру шарика, можно сравнить с тем, как сила гравитации стремится приблизить к поверхности землю плиту, установленную в вертикальных направляющих.
С этим сравнением согласны?
Если нет, то почему?
Автор: mechanic 26.12.2018, 17:01
На другой ответ я и не рассчитывал. Я имею в виду современные определения работы и теплоты в термодинамике. Иначе мы будем разговаривать на разных языках.
Автор: Patent 26.12.2018, 18:31
Вы читать не умеете или невнимательны? У меня конкретно указано - "Шарик находится в условиях, когда температура внутри шарика и снаружи едина".
При чём тут термодинамическая работа?
Автор: mechanic 27.12.2018, 6:05
С этим сравнением согласны?
Если нет, то почему?
Сходство есть, но только внешнее. Главное, и оно же качественное, отличие в количестве и размере шариков, которые выпускает ваша установка в эксперименте с плитой. Сравнивать макроскопическую систему с микроскопической некорректно. Чтобы приблизить ваш эксперимент к воздушному шарику, нужно чтобы ваша установка стреляла мельчайшми песчинками со скорострельностью ну хотя бы миллиард выстрелов в секунду. Тогда никаких практически колебаний плита не будет испытывать.
Вывод. Установка, посредством шариков совершает работу, периодически сдвигая вверх плиту.
Можно по-другому. Каждый шарик выполняет работу по перемещению плиты вверх не некую величину, отдавая ей часть своей кинетической энергии.
Не вы ли это написали? Или вот это:
Про то, что в школе относят к процессу РАБОТА.
Это ВЫ , а не МЫ разбираем школьный курс. Я, лично, на уровне школьного курса обсуждать вопросы теплоты и работы не собираюсь. Чисто механическое определение работы, как произведения силы на перемещение, непригодно для термодинамики, как, впрочем, и для электродинамики.
Чтобы в этой теме не открывать курс лекций по термодинамике, потрудитесь прочесть страницы 40-56 в книге К.А.Путилов ТЕРМОДИНАМИКА 1971, или в книге Базарова ТЕРМОДИНАМИКА 2010г. стр.14-21 и 24-27.Их можно легко скачать из электронных библиотек.
Автор: alal 27.12.2018, 9:00
Про то, что в школе относят к процессу РАБОТА.
Во-первых, при чём здесь моё понимание, если спрашивается о Вашем?
Понимание работы даётся в школьных учебниках.
Вам школьные трактовки для объяснений не подходят? Если не согласны со школьными трактовками, то дайте свои из …
Вам лучше знать - где Вы их берёте, поскольку они Ваши.
Давайте поэтапно.
Вот со своей позиции (а не с моего понимания) работы и теплоты и дайте по двум примерам чёткий ответ.
Пример 1. Установка стреляет шариками в плиту, которая установлена в вертикальных направляющих и под действием силы своей тяжести стремиться опуститься. Но это ей сделать не позволяют шарики, которыми снизу по ней стреляет соответствующая установка.
В этом случае плита совершает малые вертикальные перемещения. Чуть опуститься вниз, а после удара очередного шарика, опять сдвинется вверх. И так постоянно.
Вывод. Установка, посредством шариков совершает работу, периодически сдвигая вверх плиту.
Можно по-другому. Каждый шарик выполняет работу по перемещению плиты вверх не некую величину, отдавая ей часть своей кинетической энергии.
Пример 2. Рассматриваем фрагмент оболочки обычного воздушного шарика.
Шарик находится в условиях, когда температура внутри шарика и снаружи едина.
Рассматриваем то, что получается при этих условиях по МКТ.
Растянутая оболочка шарика стремиться сжаться. В этом случае стремление каждого фрагмента оболочки переместиться к центру шарика, можно сравнить с тем, как сила гравитации стремится приблизить к поверхности землю плиту, установленную в вертикальных направляющих.
С этим сравнением согласны?
Если нет, то почему?
Да не тяните же! Сообщите уже благую весть!
Все форумчане почти заснули или разбежались...
Кратко, четко, с расстановкой !
Автор: Patent 27.12.2018, 19:14
Дык, я же не о размере колебаний, а о их существовании в принципе.
Итак, приближаем ситуации к большему совпадению. Пусть установка стреляет мельчайшими пылинками с соответствующей скоростью.
Пусть плита почти (практически) стоит на месте. Это значит, что колебания сведены к минимуму и не видны нашему глазу. Но! Они есть! Пусть даже меньше микрона на несколько порядков. Следовательно, анализ этих условий указывает на то, что работа установки с затратами соответствующей энергии по удержанию плиты производится. С этим согласны?
А поскольку пришли к совпадению, то это означает, что при указанных условиях и в шарике должна производиться (выполняться) соответствующая работа. Вы с этим согласны?
Чтобы в этой теме не открывать курс лекций по термодинамике, потрудитесь прочесть страницы 40-56 в книге К.А.Путилов ТЕРМОДИНАМИКА 1971, или в книге Базарова ТЕРМОДИНАМИКА 2010г. стр.14-21 и 24-27.Их можно легко скачать из электронных библиотек.
Открыл данную ссылку – http://padaread.com/?book=6053&pg=44
Нарезал кучу цитат, а потом передумал их здесь размещать.
Лучше читать весь текст на этих страницах.
Вы их сами внимательно читали?
А насколько объективно оцениваете прочитанное?
Он же ничего внятного не представил. Указал на то, что большее количество учёных ошибается, а он и ещё некоторые имеют правильное видение. А своё видение ещё более непонятно представлено. Ничего внятно-конкретного. Просто указывал, что другое большинство имеет неправильное видение, а он правильное.
Прямо как Горбачёв, когда отдавал команду вырубать виноградники, подкрепляя своё решение словами «и это правильно».
Ну и как Вы с его позиции способны ответить на мои вопросы?
Мне очень интересно видеть Ваши ответы на мои вопросы с позиции Путилова.
И далее.
На стр. 46 он ссылается на опыты Румфорда и Деви.
Про то, как эти опыты можно трактовать иначе – здесь:
https://www.youtube.com/watch?v=Q87rigBQC58
Если раньше не задумывались, то задумайтесь сейчас.
На каком основании эти опыты считаются очевидным доказательством правоты МКТ? Разве кто-либо внятно представил механизм того, как относительно медленное движение кромки сверла увеличивают амплитуду колебаний атомов взаимодействующих металлов?
Увы! Вся «очевидность» начинается и заканчивается одной общей фразой, что обнаружилась несостоятельность теории теплорода. А то, что эта «несостоятельность» плод недальновидных размышлений никто ранее не задумался.
Открываем интернет на термине - «Теплород
гипотетическая тепловая материя (невесомая жидкость), присутствием которой в телах в 18-19 веках пытались объяснять наблюдаемые тепловые явления (нагрев тел, теплообмен, тепловое расширение, тепловое равновесие т.п.)».
«Теплоро́д (калька с греч. φλογιστός — пламя), Флогистон — по распространённым в XVIII — начале XIX века воззрениям, невесомый флюид, присутствующий в каждом теле и являющийся причиной тепловых явлений».
В разных источниках информация мало чем отличается от приведённой.
Заметьте, теплород везде (во всех источниках) изначально относят к невесомому флюиду.
На самом деле (о чём просто или специально забыли) элементы теплорода изначально награждались силами взаимодействия между собой и другими элементами материи. То есть, в исходных условиях элементам теплорода (далее ЭТ) предположительно задавались силы отталкивания между собой и силы притяжения к иным элементам.
А далее цепью логических рассуждений, вспоминая о существовании вулканов и гейзерах, следует констатировать то, что под земной корой, т.е. в раскалённой сердцевине Земли, размещено гигантское количество ЭТ.
Это значит, что при заданных исходных данных, элементы теплоты у тел, находящихся на земной поверхности и взаимодействующие с тем, что находится внутри земли, невесомыми флюидами никак не могут быть в принципе!
Все форумчане почти заснули или разбежались...
Кратко, четко, с расстановкой !
Тяну не я, а механик всячески уклоняется от внятных ответов.
Автор: mechanic 27.12.2018, 22:43
Позвольте господа мне, неверующему, взмолиться! У нас было Рождество, сейчас школьные каникулы, внуков негде держать, так как родители работают, да еще новогодние праздники впереди. Никто не тянет, просто времени в обрез.
Отвечу накоротке Патенту:
А поскольку пришли к совпадению, то это означает, что при указанных условиях и в шарике должна производиться (выполняться) соответствующая работа. Вы с этим согласны?
Сначела решим задачу макроскопически: На плиту действует суммарная сила давления Р, вызванная бомбардировкой частиц, на частицы действует равная по величине и противоположно направленная противодействующая сила - вес плиты. Система находится в состоянии равновесия в покое. Перемещение плиты S =0. Работа силы давления A=PS A=P*0=0.
То есть суммарная работа частиц равна нулю.
Он же ничего внятного не представил. Указал на то, что большее количество учёных ошибается, а он и ещё некоторые имеют правильное видение. А своё видение ещё более непонятно представлено. Ничего внятно-конкретного. Просто указывал, что другое большинство имеет неправильное видение, а он правильное.
А вы не обратили внимание, когда это было написано? Это были тридцатые годы прошлого столетия! Сейчас возьмите практически любой серьезный учебник по термодинамике и увидите, что увидите то же самое о чем писал Путилов в 1937м.
Следующий вопрос:
И далее.
На стр. 46 он ссылается на опыты Румфорда и Деви.
Про то, как эти опыты можно трактовать иначе – здесь:
В опыте Румфорда количество теплоты, выделившейся при сверлении в точности соотвествует количеству произведенной работы. Добыть такое же количество тепла из окружающей среды путем телообмена за это же время невозможно, да и температура ее ниже. Опыт Румфорда находится в полном согласии с законом сохранения энергии (Первым началом термодинамики).
В опыте Дэви в вашем рассуждении (по ссылке) заложена грубейшая ошибка. Вы не учли главный потребитель энергии - скрытую теплоту плавления льда, которая почти на два порядка выше разницы в телоемкостях льда и воды. Чтобы растопить 1килограмм льда необходимо про постоянной температуре затратить 80 ккал тепла, а чтобы нагреть тоже количество воды на один градус необходимо затратить всего одну килокалорию. У меня времени больше нет, а я не получил от вас ответа, что собой представляют понятия теплота и работа в свете прочитанного у Путилова.
Автор: mechanic 4.1.2019, 6:49
Что- то не видно и не слышно моих оппонентов. То ли не отошли от новогодних возлияний, то ли Patent углубился в изучение термодинамики, чтобы ответить на заданные вопросы.
А пока я вкратце напомню основные тезисы изложенного.
Термодинамической системой называется выделенная часть пространства или тело, отделенная реальной или воображаемой оболочкой от окружающей внешней среды. (определение)
Большинство химически устойчивых веществ в зависимости от параметров термодинамической системы ( Давление, объем, температура и т.д.) могут находиться в трех агрегатных состояниях : твердом, жидком, и газообразном
В твердом состоянии вещество сохраняет свою форму, в жидком в отсутствии силы тяжести принимает форму шара, а при наличии силы тяжести - принимает форму сосуда и обладает поверхностью раздела, отделяющую ее от других фаз.
В отличие от жидкостей и твердых тел газы не имеют формы и запоняют все отведенное для них пространство.
Твердые тела делятся на два типа: истинно твердые , то есть кристаллические тела, молекулы или атомы которых образуют кристаллическую решетку, и тела аморфные, по своей структуре и по большинству свойств предствляющие застывшие очень вязкие жидкости.
Термодинамически различные агрегатные состояния вещества различаются уровнем внутренней энергии. Между истинно твердым состоянием вещества и жидким существует энергетический барьер, называемый скрытая теплота плавления (кристаллизации), а между жидким и газообразным состоянием есть энергетический барьер, который имеет название скрытая теплота парообразования. (Продолжу завтра)
Автор: Digger 4.1.2019, 14:17
Эт-т вы, наверное, всё ещё отмечаете крисмас, ежели до сих пор не удосужились ответить на мой вопрос, касающийся механизма теплового излучения, заданный вам две недели тому назад:
http://"http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164780
Вот он:
"Если по существующей теории (МКТ) вся тепловая энергия газа - это сумма кинетических энергий атомов и молекул, то откуда берётся энергия теплового излучения?
Между соударениями молекулы газа излучать не могут в принципе, поскольку, во-первых, электрически =lruнейтральны, а, во-вторых, движутся равномерно и прямолинейно, а, в момент соударения тоже излучать не могут, поскольку соударение по МКТ абсолютно упругое, т.е. происходит без потерь".
Автор: mechanic 4.1.2019, 17:20
#158
Этот вопрос не в тему.
Автор: Digger 4.1.2019, 17:40
Понятно, ответа нет и не будет...
Автор: Patent 4.1.2019, 18:53
Отвечу накоротке Патенту:
Сначела решим задачу макроскопически: На плиту действует суммарная сила давления Р, вызванная бомбардировкой частиц, на частицы действует равная по величине и противоположно направленная противодействующая сила - вес плиты. Система находится в состоянии равновесия в покое. Перемещение плиты S =0. Работа силы давления A=PS A=P*0=0.
То есть суммарная работа частиц равна нулю.
Вы здесь желаемое выдаёте за действительное.
Общее перемещение можно (наплевав на неудобное) приравнять к нулю.
Но!!!!!
Вы мозг включите!
Если система находится по действием ЧЕРЕДУЮЩИХСЯ УДАРОВ снизу и статической силы сверху вниз, то хотите вы этого или НЕ хотите, а колебания должны присутствовать. Хоть чрезвычайно мизерные, но присутствовать!
Отсутствие колебаний будет если статической силе противостоит статическая! то есть как по ТТЭ.
Я выше
здесь - http://xn----8sbbemc3a7aecex.xn--p1ai/forum/index.php?s=&showtopic=87610&view=findpost&p=2164796
я спрашивал Вас - "А теперь честно сопоставьте, если по ТТЭ в воздушном шарике статической силе снаружи противостоит статическая сила изнутри, то это лучший вариант или нет?"
Почему вы проигнорировали этот мой вопрос?
Следовательно, вы признаёте, что ничего путного нет ни там, ни там.
Автор: mechanic 4.1.2019, 21:23
А я к тому, чтобы не засоряли тему оффтопом. Есть топики по термодинамике электромагнитному излучению. Туда и пишите.
Следовательно, вы признаёте, что ничего путного нет ни там, ни там.
А вы хоть поняли о чем идет речь? Поясните, но не в этой теме, а в Термодинамике.
Это тоже оффтоп. Ответ будет в термодинамике, но прежде всего ответьте мне уже в тему Термодинамика на вопрос: чем отличаются консервативные силы от диссипативных?
Автор: ahedron 4.1.2019, 22:31
Вот вам крест на МКТ... очень простой опыт, поджигаете спичку и немного погодя тушите её - поднимается дым... И о чудеса - ничто, никуда не разлетается, а поднимается медленной "струйкой", немного охладившись, дым начинает "падать", а уже потом - рассеиваться.
mechanic, Что пишут в книжках по этому поводу? Что дым это не газ?)
Автор: vps137 5.1.2019, 3:18
mechanic, Что пишут в книжках по этому поводу? Что дым это не газ?)
Этот опыт из неравновесной термодинамики. В этой части, мне кажется, ещё много чего непознанного. Традиционная термодинамика изучает замкнутые системы.
Здесь в опыте курильщика, как мне кажется, МКТ вполне работает. Частиц дыма, напр. смеси никатина со всякой дрянью, что Вы вдыхаете при курении, рассеивает хаотическое движение молекул тех газов, из которых состоит воздух. Дым от потушенной спички, конечно, нагрет, потому и поднимается вверх.
Автор: mechanic 5.1.2019, 5:53
mechanic, Что пишут в книжках по этому поводу? Что дым это не газ?)
Откройте книжку под названием Химия и получите ответ. Если не найдете - открывайте тему. Это не сюда. А креститься лучше в церкви.
А я продолжу пост 172.
Поясню процесс изменения агрегатного состояния на примере жидкость - твердое тело.
[attachment=278:p0509__3_.jpg]
На рисунке 450 показан график затвердевания кристаллического тела в коодинатах время (тау) - температура (Т) при постоянном отводе тепла Слева- направо мы видим нисходящую кривую, характеризующую охлаждение жидкости, затем горизонтальную прямую - изотерму кристаллизации и снова нисходящую кривую - охлаждение твердого тела. О чем говорит горизонтальный участок линии охлаждения. Отвод телоты продолжается, а температура не падает! Она не падает по одной причине: при затвердевании выделяется энергия кристаллизации, которая и поддерживает температуру постоянной. Она равна той энергии, которую в свое время затратили на плавление (скрытая теплота плавления).
На рисунке 451 показан график затвердевания аморфного тела. Он практически ничем не отличается от процесса охлаждения и загустевания жидкости.
О чем это говорит? Это говорит только о том, что тела кристаллического строения обладают меньшей внутренней энергией, чем жидкость при той же температуре на величину скрытой теплоты плавления (кристаллизации). Этот опытный факт показывает, что не все так просто обстоит в процессе изменения агрегатного состояния. Нельзя в одну бочку бросать якобы твердые аморфные вещества и истинно твердые - кристаллические. Одного и того же объяснения изменения агрегатного состояния на молекулярном уровне у них нет и не может быть. Точно также не может быть одного объяснения перехода из жидкого состояния в газообразное. Общее понятие - Ван-дер-Ваальсовские силы притяжения , взятое из термодинамики притяжения, возникающие в парах и жидкостях при сближении, атомов и молекул. на молекулярном уровне имеют совершенно различное происхождение, зависящее от строения молекул, взаимосвязях атомов в молекулах и взаимосвязях молекул (или отдельных атомов) между собой.
Завершая термодинамический взгляд на агрегатные состояния вещества, необходимо отметить, что есть обходной путь перевода вещества из твердого состояния в жидкое и газообразное минуя фазовые переходы: плавление (кристаллизацию), испарение (конденсацию) через закритическую область. Но об этом, при желании, можно поговорить в теме Термодинамика.
В следующем посте я постараюсь резюмировать все, что было сказано об агрегатных состояниях вещества с позиции молекулярной теории строения вещества.
Автор: Digger 5.1.2019, 7:36
Т.е. процесс (тепловое излучение), который невозможно внятно объяснить с позиций МКТ, в которой вся! тепловая энергия - суть кинетическая энергия движущихся атомов и молекул - оффтоп?
Обычное поведение страуса, прячущего голову в песок при виде опасности...
Вопрос о том, откуда берётся энергия теплового излучения, демонстрирует несостоятельность МКТ, зиждящейся не на экспериментальном измерении скоростей молекул газа при н.у., а на притянутом за уши постулате о том, что тепловая энергия - это только кинетическая энергия движущихся атомов и молекул.
Т.е. МКТ даёт искажённое представление о природе теплоты.
ТОЧКА.
Автор: mechanic 5.1.2019, 20:53
Читайте название темы. Это оффтоп. Обсуждать ваш вопрос в этой теме не собираюсь. Перенесите в термодинамику. Точка.
Автор: mechanic 12.1.2019, 6:17
mechanic, Что пишут в книжках по этому поводу? Что дым это не газ?)
Отвечу коротко, хотя вопрос не по теме. Опыт со спичкой простой только на первый взгляд. Во- первых при горении происходят химические процессы окисления, сопровождающиеся выделением энергии. Содержащийся в древесине водород соединяется с кислородом воздуха образует водяной пар H2O, а углерод. соединяясь с кислородом, образует углекислый газ-CO2. Из-за неполного сгорания образуется также угарный газ CO и углерод в виде мелких частиц угля, составляющих основную часть дыма. Дым это коллоидная система -смесь воздуха с мелкодисперстным твердым веществом. Нагретый в результате горения дым - легче воздуха. Он поднимается вверх. По мере остывания плотность дыма увеличивается, и, когда дым становится тяжелее воздуха он опускается, затем рассеивается благодаря броуновскому движению.
Автор: Digger 12.1.2019, 20:28
Масса частицы дыма в тысячи раз больше массы молекулы воздуха.
Как частичка дыма может быть легче воздуха?
Почему при остывании дым становится тяжелее воздуха?!
И ещё:
Кто, где и когда обнаружил броуновское движение в воздухе?
В 1827 году Броун открыл движение пыльцевых зёрен в жидкости (позднее названное его именем). Исследуя пыльцу под микроскопом, он установил, что в растительном соке плавающие пыльцевые зёрна двигаются совершенно хаотически зигзагообразно во все стороны.
А кто наблюдал хаотическое и зигзагообразное движение взвешенных частиц в воздухе?
Форум Invision Power Board (http://nulled.cc)
© Invision Power Services (http://nulled.cc)
